
Две основные реакции
Мы возвращаемся к основному вопросу этой главы: какова судьба ионов после их образования в результате фотоионизации? Раз динамическими процессами на выбранных нами высотах можно пренебречь, следует рассмотреть фотохимические реакции. Двумя главными типами химических процессов на высотах 100 - 200 км являются (кроме фотоионизации) диссоциативная рекомбинация и ионно-молекулярные реакции. О них-то мы и поговорим, прежде чем перейти к общей картине ионных преобразований.
В книге "Химия, ионосфера и космос" подробно рассказано об истории становления взглядов на диссоциативную рекомбинацию молекулярных ионов как быстрый процесс, играющий важную роль в ионосфере Земли и планет. Понадобилось около 20 лет, чтобы от первых предположений английского ученого Бейтса о существовании и роли диссоциативной рекомбинации прийти к современным представлениям об этом процессе.
Итак, диссоциативная рекомбинация молекулярных ионов. Она записывается в виде
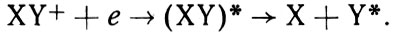
Формула 10
При соединении молекулярного иона XY+ с электроном, как и при всякой рекомбинации, выделяется энергия, которая ранее была затрачена на ионизацию. От того, какие есть пути уноса этой энергии, будет зависеть эффективность (константа скорости) данного типа рекомбинационных процессов. В реакциях (6) и (7) энергия уносится либо излучением (отсюда и название "радиативная рекомбинация", (6)), либо третьей частицей М (реакция тройных соударений (7)). Это малоэффективные пути уноса энергии, поэтому и эффективность процессов (6) и (7) мала.
В процессе диссоциативной рекомбинации (10) энергия рекомбинации тоже сначала идет на возбуждение. Но образующаяся молекула нестабильна: она не может удержать полученный запас энергии и распадается на составляющие ее атомы, один из которых в свою очередь может быть возбужден.
Такой путь освобождения энергии, выделяющейся при рекомбинации, более всего удобен природе - константа скорости диссоциативной рекомбинации весьма высока. Если для процесса радиативной рекомбинации (6), как мы видели, константа скорости равна 10-12 см3×с-1, то для процессов диссоциативной рекомбинации основных ионосферных ионов она составляет 10-6-10-7 см3×с-1. Разница в миллион раз и определяет ту важную роль, которую процесс диссоциативной рекомбинации играет в ионосфере как главный рекомбинационный процесс выше 100 км.
Что же мы знаем и чего не знаем сейчас о конкретных процессах диссоциативной рекомбинации?
В ионосфере нас интересует главным образом диссоциативная рекомбинация трех основных молекулярных ионов NO+, О2+ и N2+:
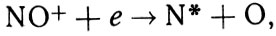
Формула 11
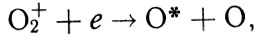
Формула 12
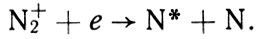
Формула 13
О рекомбинации сложных ионов-связок, наблюдаемых в области D, мы поговорим в одной из следующих глав. Для ионов N2+, О2+ и NO+ было проведено много лабораторных измерений. Трудности таких измерений и забавные случаи, которые при этом возникали, описаны в книге "Химия, атмосфера и космос". К настоящему времени эти трудности преодолены - мы имеем надежные значения констант диссоциативной рекомбинации для наших ионов (обозначим их соответственно αN0+, αО2+ и αN2+) при комнатной температуре (около 300 К):
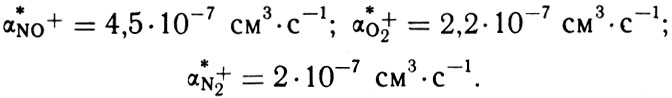
Формула 14
Однако температура 300 К не характерна для верхней атмосферы. Для интересующих нас высот более характерны температуры 1000 К и выше. Значит, нужно еще знать, как меняются величины α* с температурой. Но тогда возникает следующий вопрос: с какой именно температурой? Ведь в реакции участвуют ион и электрон, а температура ионов и электронов в ионосфере может быть различной. А может, вообще, величины α* зависят от температуры основной массы частиц среды, т. е. от температуры нейтралов?
Полностью этот вопрос не решен и по сей день. При лабораторных измерениях, которые, собственно, и питают нас сведениями о скоростях диссоциативной рекомбинации для различных ионов, получают несколько разную картину изменения α* в зависимости от того, меняют ли в эксперименте только электронную температуру Те при неизменных ионной температуре Ти и температуре нейтралов Тн или увеличивают Те и Ти одновременно. Принято все же считать (и это является основой всех аэрономических расчетов), что в первую очередь величины α* зависят от температуры электронов. Для ионов NO+ и О2+ принимается обратно пропорциональная зависимость α* от Те, а для N2+ зависимость оказалась настолько слабой, что ею часто пренебрегают. Таким образом, в основной части ионосферы мы имеем три процесса диссоциативной рекомбинации (11) - (13) с константами скорости:
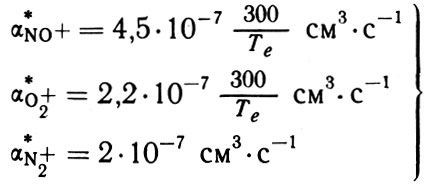
Формула 15
Казалось бы, выражения (15) дают нам исчерпывающий ответ на все вопросы, связанные с диссоциативной рекомбинацией молекулярных ионов в ионосфере. На любой высоте, в любых условиях, зная электронную температуру, можно вычислить α* для любого из ионов. И действительно, знание величин α* в виде (15) считалось бы вполне достаточным 10 лет назад. Но, увы, не сегодня - ведь аэрономия не стоит на месте.
На два вопроса мы не получаем ответа, имея выражения (15). Первый - что будет, если ионы находятся в возбужденном состоянии? Все измерения в лаборатории проводятся для невозбужденных ионов. А в ионосфере, как мы теперь понимаем, часть ионов может образовываться с запасом внутренней энергии - возбуждением. Как это отразится на эффективности диссоциативной рекомбинации, мы пока не знаем. Есть лишь общие соображения о том, что величины α* для возбужденных ионов должны быть ниже и могут составлять даже 10-8 см3×с-1. Иначе говоря, возбужденные ионы должны быть более долгоживущими, чем обычные. Если это так, то даже небольшая доля возбужденных ионов (скажем, 10%) может приводить к заметному, в 2 раза, увеличению равновесной концентрации ионов. А это очень существенно.
Второй вопрос тоже связан с возбуждением. Но уже продуктов реакции (11) - (13)-атомов кислорода и азота. В большинстве случаев один или оба продукта диссоциативной рекомбинации должны "быть возбуждены. Но в какое состояние? (Скажем, атом кислорода будет в состоянии 1D или 1S?) И какой из атомов? Пойдет ли реакция диссоциативной рекомбинации NО+ по пути (11) с образованием возбужденного атома азота или по пути NO++е→N + O* С образованием возбужденного атома кислорода?
Мы не будем сейчас говорить о том, почему важно знать ответы на эти вопросы. Отметим лишь, резюмируя положение дел с диссоциативной рекомбинацией, что основными сведениями об этом процессе, необходимыми для анализа всего цикла процессов ионизация - рекомбинация, мы располагаем, ну а отсутствие данных о возбуждении продуктов - атомов азота и кислорода - порождает свои проблемы в другой области: в физике малых составляющих и возбужденных частиц, о которых мы поговорим позже.
Выражение "ионно-молекулярные реакции" стали употреблять в аэрономии около 10 лет назад. До того использовали термины вроде "перезарядка", "перенос зарядов", которые и сейчас изредка встречаются в литературе.
Что же стоит за выражением "ионно-молекулярные реакции"? Эти реакции объединяют несколько типов процессов. Не вдаваясь в детали химической кинетики, приведем характерные примеры в виде тех реакций, которые понадобятся нам в дальнейшем:
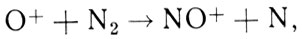
Формула 16
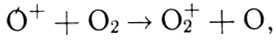
Формула 17
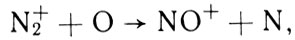
Формула 18
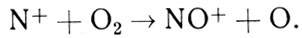
Формула 19
Несмотря на заметные различия, у этих реакций много общих черт. В каждой реакции участвуют заряженная (положительный ион) и нейтральная частицы и получаются заряженная и нейтральная частицы. Значит, ни образования, ни исчезновения зарядов не происходит. Происходит их перераспределение. В этом отличие ионно-молекулярных реакций от процессов ионизации, где заряженные частицы образуются, и от рекомбинационных процессов, где они гибнут.
Вторая важная особенность ионно-молекулярных реакций состоит в том, что слева всегда стоит ион с большим потенциалом ионизации, чем справа. Это необходимо для того, чтобы реакция не требовала дополнительной энергии, т. е. была, как говорят, экзотермической. Если же это условие нарушить, то мы получим реакцию, которая для своего протекания требует подпитки энергии извне, т. е. является эндотермической. Такие процессы, как правило, идут медленно и большой роли в аэрономии не играют. Требование экзотермичности приводит к тому, что в аэрономических ионно-молекулярных реакциях чаще всего образуются ионы N0+ и O2+, редко - ионы О+ и никогда не образуются ионы N2+.
Стоит обратить внимание еще на одну характерную деталь. Из четырех процессов, которые мы выбрали для примера, два содержат в правой части атомы азота, а в левой - молекулы N2. Значит, ионно-молекулярные реакции кроме перераспределения ионов могут приводить и к диссоциации молекул (скажем, N2) на атомы. Для кислорода это почти несущественно, а вот для образования атомного азота... Но об этом мы поговорим в одной из следующих глав.
Нас, как всегда, в первую очередь интересует эффективность данного типа процессов, т. е. константы скорости ионно-молекулярных реакций. Нужно отметить, что разброс значений у для различных ионосферных реакций гораздо больше, чем разброс значений α*. Как мы только что видели, для константы диссоциативной рекомбинации при 300 К разница между быстро рекомбинирующим ионом окиси азота и медленно рекомбинирующим ионом N^ относительно невелика - два с небольшим раза. А в случае ионно-молекулярных реакций диапазон у при комнатной температуре достигает двух порядков величины - от 10-12 см3×с-1 до 10-10cм3×c-1.
Но важно, конечно, не это, а то, знаем ли мы эти константы достаточно надежно, чтобы использовать их для аэрономических расчетов? В целом на этот вопрос сегодня следует ответить утвердительно. После многих лет поисков, споров и ошибок мы знаем сейчас величины γ для основных ионно-молекулярных реакций и их зависимость от температуры. Как ионно-молекулярные реакции вписываются в общий цикл процессов, мы увидим в следующем параграфе, а сейчас расскажем о проблеме, показывающей, насколько сложны вопросы, связанные с ионно-молекулярными реакциями.
Есть такое понятие - "колебательная температура", или "температура колебательного возбуждения". Дело в том, что практически при любой температуре газа часть молекул этого газа будет находиться в состоянии колебательного возбуждения. С ростом температуры количество колебательно возбужденных молекул быстро растет. Однако возможна ситуация, когда температура газа не меняется, а количество (процент) колебательно возбужденных частиц растет (скажем, за счет фотохимических процессов). В этом случае рост числа возбужденных частиц можно приписать росту некоторой эффективной температуры - температуры колебательного возбуждения Тк. В самом простом случае Тк просто равна обычной (кинетической) температуре газа Тн. В остальных случаях (при наличии дополнительных источников возбуждения) Тк больше, чем Т н.
Группой американских исследователей под руководством Фергюсона, заложивших основы наших сегодняшних представлений о величинах γ, в 1969 году был получен неожиданный результат.
Колебательная температура
Оказалось, что константа самой важной ионосферной ионно-молекулярной реакции (16) зависит от колебательной температуры участвующих в ней молекул азота. Причем не просто зависит, а очень сильно зависит. При изменении Тк от 300 до 1000 К константа γ16 возрастала в 100 (!) раз.
Этот факт получил огромный резонанс среди специалистов по аэрономии. Возник вопрос о пересмотре чуть ли не всей схемы ионизационно-рекомбинационных преобразований в ионосфере. Однако до этого дело пока не дошло. При внимательном подходе выяснилось, что такой драматический эффект получается, когда сам газ остается холодным, при комнатной температуре. А при температуре, скажем, 1000 К увеличение колебательной температуры уже не ведет к росту γ16 более чем в 2 раза. А поскольку нас в ионосфере интересуют как раз температуры Тн в 1000 К и выше, эффект колебательного возбуждения не должен как будто играть такой страшной роли, как показалось сначала.
Однако проблема не снята с повестки дня. Дело в том, что для объяснения ряда эффектов в области F2 ионосферы требуется предполагать зависимость константы реакции (16) от условий. Но от каких? Все от той же колебательной температуры азота? Или, может быть, как предложили недавно, от электронной температуры, которая сильно меняется на высотах максимума F2? Ответ еще предстоит найти.
|
ПОИСК:
|
© GEOMAN.RU, 2001-2021
При использовании материалов проекта обязательна установка активной ссылки:
http://geoman.ru/ 'Физическая география'
При использовании материалов проекта обязательна установка активной ссылки:
http://geoman.ru/ 'Физическая география'