
6. Группа углерода
Относящиеся сюда минералы также занимают особое положение среди самородных элементов. Эта группа представлена двумя резко различными по физическим свойствам полиморфными модификациями углерода: алмазом и графитом.
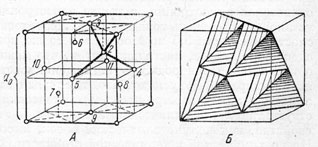
Рис. 81. Кристаллическая решетка алмаза. А - изображение центров атомов; В - та же решетка в виде тетраэдров, вершины и центры которых являются центрами атомов углерода
Кристаллическая структура алмаза (рис. 81) в целом как бы похожа на структуру гранецентрированного куба, но отличается от нее тем, что атомы углерода располагаются не только на гранях куба, но также в центрах половинного числа малых кубов, чередующихся с пустыми малыми кубами. Более наглядно эта структура показана на рис. 81-Б в виде комбинации тетраэдров, в которых кроме четырех атомов по вершинам в центре располагается пятый атом (рис. 82-В). Каждая вершина тетраэдра является общей для четырех смежных тетраэдров.
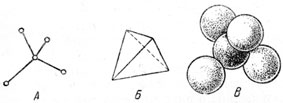
Рис. 82. Разные способы изображения тетраэдрического расположения атомов . Расстояния центров атомов во всех трех фигурах одинаковы
Обычно представляют, что атомы углерода в кристаллической структуре алмаза соединены друг с другом исключительно ковалентными связями по направлениям, соединяющим центр тетраэдра с его вершинами. Однако Н. В. Белов развил более естественное представление о структуре алмаза, как о структуре типа ZnS с двумя сортами ионов-С4+ и С4- (радиус катиона С4+ составляет около 0,15, а аниона О4--около 1,5Å), что обусловливает плотнейшую упаковку анионов в структуре. С таким представлением хорошо увязываются гемиэдрические черты кристаллов алмаза и ряд таких свойств, как бесцветность, низкая электропроводность, необычайно высокая твердость*, весьма высокая устойчивость при широких колебаниях температуры и давления (в частности, при нагреве до температуры 2500° в отсутствии кислорода не обнаруживает никаких изменений), очень высокая устойчивость по отношению к кислотам и щелочам и др.
*(Необычайная физическая прочность алмаза, с точки зрения законов квантовой механики, в данной структуре обусловливается непрерывной осцилляцией, выражающейся в превращении отрицательных в данный момент ионов в положительные в следующий момент и наоборот)
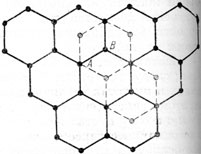
Рис. 83. Расположение центров атомов в листах решетки графита. Каждый следующий лист как бы сдвинут на расстояние в половину диаметра шестерных колец
Структура графита весьма существенно отличается от структуры алмаза Ионы углерода в графите лежат листами, представленными плоскими гексагональными сетками (рис. 83). По Н. В Белову, кристаллическая структура графита представляет плотнейшую упаковку крупных анионов С4-, в которой половина треугольников в каждом листе занята маленькими катионами С4+*. Каждый ион в плоской сетке окружен тремя соседними ионами на расстоянии 1,42Å (в алмазе 1,54Å), расстояние же между плоскими сетками 3,40Å, т. е. в два раза больше. Отсюда становится понятным ряд свойств графита: его значительно меньший удельный вес по сравнению с алмазом, чрезвычайно легкая расщепляемость на тонкие чешуйки, резко выраженная оптическая анизотропия, а также анизотропия твердости, которую удается установить при очень точных тонких исследованиях (перпендикулярно к плоскости спайности 5,5 по Моосу, а в то же время, благодаря очень слабому сцеплению листов, настолько мягок, что мажет бумагу и пальцы). Этим же объясняется неоднородность поглощения света, чем и обусловлен черный цвет минерала. Допускают, что тип связи атомов в графите, в отличие от алмаза, в какой-то мере носит металлический характер, т. е. в связях участвуют также "металлические" электроны. С этим вполне увязываются такие свойства, как полуметаллический блеск, высокая электропроводность и др. Но по химической и термической стойкости графит все же близок к алмазу.
*("Как и в алмазе, происходит непрерывная осцилляция те ионы, которые в течение диференциала времени были катионами, в следующий диференциал становятся анионами Резонанс двух геометрически тождественных структур приводит к еще большему по сравнению с алмазом укорочению расстояния между центрами атомов С (1,42 вместо 1,54Å) Центры тяжести атомов С, если не различать между катионами и анионами, дают сетку из правильных шестиугольников" (Н. В. Белов))
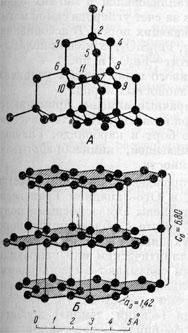
Рис. 84. Расположение центров атомов в алмазе (А), при горизонтальном расположении плоских сеток (111), и в графите (Б)
Если мы решетку алмаза изобразим в таком виде, как это показано на рис. 84-А, т. е. вдоль тройной оси (ср. номера атомов на рис. 81-А), то в горизонтальных плоских сетках также заметим гексагональные кольца (атомы 6,11, 8, 9, 7 и 10), с той лишь разницей, что эти сетки не совсем плоские: три атома располагаются несколько выше по сравнению с другими тремя. Этим и объясняется, почему в кристаллах алмаза спайность средняя по {111}, тогда как в графите-по {0001} совершенная.
Алмаз - С. Название происходит от греческого слова "адамас" - непреодолимый (очевидно, имелись в виду его наивысшая твердость и устойчивость по отношению к физическим и химическим агентам).
Разновидности:
- борт - неправильной формы сростки и шаровидные лучистые агрегаты;
- карбонадо - тонкозернистые пористые агрегаты, окрашенные аморфным графитом и посторонними примесями в буровато-черный цвет.
Химический состав. Бесцветные разновидности состоят из чистого углерода. Окрашенные же и непрозрачные разновидности в несгораемом остатке, достигающем иногда нескольких процентов, обнаруживают SiO2, MgO, CaO, FeO,Fe2O3, A12O3, ТiO2 и др. В виде включений в алмазах нередко наблюдается графит и некоторые другие минералы.
Сингония кубическая; гексатетраэдрический в. с. 3L424L36P.
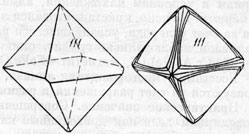
Рис. 85. Кристаллы алмаза октаэдрического облика
Облик кристаллов октаэдрический (рис. 85), менее обычен додекаэдрический; редко кубический и изредка тетраодрический (рис. 86). Характерные формы: {111}, {100} и {11О}. Грани кристаллов часто бывают представлены выпуклыми и неровными, иногда разъеденными поверхностями. Наблюдаются двойники срастания по (111), реже по (100). Размеры отдельных кристаллов варьируют от мельчайших до очень крупных, весящих несколько сот и даже тысяч каратов (метрический карат = 0,2 г). Крупнейшие кристаллы весили (в каратах): "Коллинан" - 3025, "Эксцельзиор" - 969,5, "Виктория" - 457, "Орлов" - 199,6 и др.
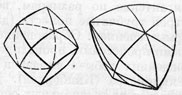
Рис. 86. Кристаллы алмаза ромбо-додекаэдрического и тетраэдрического облика
Цвет. Бесцветный водяно-прозрачный или окрашенный в голубой, синий, желтый, бурый и черный цвета. Блеск сильный алмазный. Показатель преломления N = 2,40 -2,48.
Твердость 10. Абсолютная твердость в 1000 раз превышает твердость кварца и в 150 раз - корунда. Хрупок. Спайность средняя по {111}. Уд. вес 3,47-3,56. Электропроводность слабая.
Диагностические признаки. Алмаз является единственным минералом по своей исключительной твердости. Характерны также сильный алмазный блеск и часто кривоплоскостные грани кристаллов. Мелкие зерна в шлихах легко узнаются по люминесценции, резко проявляющейся в ультрафиолетовых лучах. Цвета люминесценции обычно голубовато-синие, иногда зеленые.
Происхождение. Коренные месторождения генетически связаны с ультраосновными глубинными изверженными породами: перидотитами, кимберлитами и др. В этих породах кристаллизация алмаза происходит, очевидно, на больших глубинах в условиях высоких температур и давления. Судя по формам и условиям нахождения, алмаз кристаллизовался в магмах одним из первых. Не ясно, кристаллизовался ли алмаз за счет углерода самой магмы или за счет углерода, усваивавшегося из окружающих пород. В ассоциациях с алмазом наблюдались: графит, оливин - (Mg, Fe)2SiO4, хромшпинелиды - (Fe,Mg)(Cr,Al,Fe)2O4, магнетит - FeFe2O4, гематит - Fe2O3 и др.
Россыпные месторождения алмаза, устойчивого в экзогенных условиях, образуются за счет разрушения и размыва алмазоносных пород.
Практическое значение. Совершенно прозрачные алмазы применяются в ювелирном деле как драгоценные камни (бриллианты). Для технических целей употребляются мелкие алмазы, а также борт и карбонадо. Главным образом они используются в металлообрабатывающей, камнеобрабатывающей, абразивной и прочих отраслях промышленности.
Месторождения. Крупнейшие в мире месторождения алмазов известны в ряде районов Южной Африки: по р. Вааль, в Юго-Западном Трансваале и на юго-западном берегу Африки. Они представлены алмазоносными полуразложенными кимберлитами, заполняющими вместе с обломочными породами гигантские по размерам, вертикально уходящие вниз на несколько километров трубчатые полости (диатремы) с эллиптическим или неправильной формы сечением. Образование этих диатрем связывают с грандиозными взрывными процессами, происходившими на больших глубинах. В некоторых месторождениях добыча алмаза в настоящее время происходит с глубины свыше километра (Кимберлей). Добытая руда ("синяя земля") дробится и промывается на специальных обогатительных фабриках. Содержание алмаза в породе составляет 0,000052% (по весу). Отсюда происходят самые крупные алмазы в мире ("Коллинан", "Эксцельзиор" и др.). Кроме коренных месторождений, в Юго-Западной Африке широко распространены также богатые россыпи в системах pp. Вааль и Оранжевой. Большая добыча алмазов производится также в Бельгийском Конго.
Россыпные месторождения алмазов известны в Бразилии (Минас-Жерайж), в Индии, где ведется добыча с древнейших времен и откуда происходят крупные алмазы "Орлов", "Кохинур", и др.
Графит - С. Название происходит от греческого слова "графо" - пишу. Разновидности:
- графитит - скрытокристаллическая разность,
- шунгит - аморфная разность, образовавшаяся, повидимому, в результате природного коксования углей.
Химический состав графита редко отличается чистотой. В значительных количествах (до 10-20%) часто присутствует зола, состоящая из различных компонентов (SiO2, Аl2O3, FeO, MgO, СаО, Р2О5, CuO и др.), иногда вода, битумы и газы (до 2%).
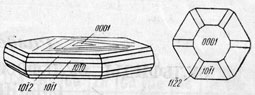
Рис. 87. Кристаллы графита
Сингония гексагональная; дигексагонально-дипирамидальный в. с. L66L27PC. Кристаллическая структура описана выше. Облик кристаллов. Хорошо образованные кристаллы встречаются крайне редко. Они имеют вид шестиугольных пластинок или табличек (рис. 87), иногда с треугольными штрихами на грани (0001). Характерные формы: {0001}, иногда {1011}, {1122} и др. Агрегаты часто тонкочешуйчатые. Реже распространены шестоватые или волокнистые массы.
Цвет графита железно-черный до стально-серого. Черта черная блестящая. Блеск сильный металловидный; скрытокристаллические агрегаты матовые. Оптически отрицателен. Показатель преломления Nm==l,93-2,07. В тончайших листочках просвечивает серым цветом.
Твердость 1. В тонких листочках гибок. Жирен на ощупь. Мажет бумагу и пальцы. Спайность совершенная по {0001}. Уд. вес 2,09-2,23 (изменяется в зависимости от степени дисперсности и наличия тончайших пор), у шунгита 1,84-1,98. Прочие свойства. Обладает высокой электропроводностью, что обусловлено очень плотной упаковкой атомов в листах.
Диагностические признаки. Легко узнается по цвету, низкой твердости и жирности на ощупь. От сходного с ним молибденита (MoS2) отличается более темным железно-черным цветом и более слабым блеском.
П. п. тр. не плавится. При накаливании в струе кислорода сгорает труднее, нежели алмаз. Улетучивается, не плавясь, лишь в пламени вольтовой дуги. В кислотах не растворяется. Порошок в смеси с KNO3 при нагревании дает вспышку.
Происхождение. В природе графит образуется при восстановительных процессах в условиях высоких температур.
Встречается иногда среди магматических горных пород разнообразного состава. Источником углерода во многих случаях являются вмещающие углеродсодержащие горные породы.
Известны случаи находок графита в пегматитах. Встречаются месторождения на контактах известняков с изверженными породами в провинциях Онтарио и Квебек в Канаде, а также жильные месторождения крупнолистоватого графита, например на о. Цейлон.
Широко распространены метаморфические месторождения графита, возникшие за счет каменных углей или битуминозных отложений в условиях регионального метаморфизма или под влиянием интрузий магмы.
Практическое значение. Графит применяется для самых различных видов производства: для изготовления графитовых тиглей, в литейном деле, производстве карандашей, электродов, для смазки трущихся частей, в красочной промышленности и др.
Месторождения. К числу крупных месторождений графита в СССР относится Алиберовское в Тункинских горах. Графит залегает среди изверженных пород (сиенитов) в виде штоков и представляет собой смесь прекрасного по качеству чешуйчатого или мелкокристаллического графита с магматическими минералами (микроклином, нефелином и др.). Местами по окраинам эти тела сопровождаются грубозернистым известняком. Сами магматические породы также содержат графит. Очень интересны графитовые образования типа секреций, распространенные среди плотных масс графита. Эти неправильной формы тельца имеют наружную корочку из тангенциально ориентированных чешуек и радиальнолучистое строение внутренней части. Образование графита связывают с восстановлением окиси углерода, выделявшейся при поглощении магмой известняков.
Вдоль северо-западного побережья Азовского моря (севернее городов Жданова и Осипенко) и в других местах Украины разрабатываются вкрапленные крупночешуйчатые графитовые руды, залегающие в виде выветрелых на поверхности пластов в древних метаморфических породах - гнейсах. Интересно, что секущие пегматитовые и аплитовые жилы в зальбандах содержат крупнокристаллические гексагональные индивиды графита, а в центральной зоне-мелкокристаллические выделения.
|
ПОИСК:
|
© GEOMAN.RU, 2001-2021
При использовании материалов проекта обязательна установка активной ссылки:
http://geoman.ru/ 'Физическая география'
При использовании материалов проекта обязательна установка активной ссылки:
http://geoman.ru/ 'Физическая география'