
5. Группа серы
Сюда относятся самородные элементы VI группы таблицы Менделеева: сера, селен и теллур. Из них сера является типичным металлоидом, тогда как селен и, особенно, теллур обладают свойствами полуметаллов.
Для самой серы устанавливаются три полиморфные модификации, из которых в природных условиях устойчивой является лишь ромбическая модификация-α-сера. При атмосферном давлении и температуре выше 96,5° она переходит в β-серу моноклинной сингонии, а при охлаждении вновь возвращается в прежнее кристаллическое состояние. γ-сера также моноклинная, но неустойчива при атмосферном давлении при всех температурах; при комнатной температуре превращается в α-серу. Другие три искусственно полученные полиморфные модификации серы в природных условиях не встречаются.
Сера - S. Наиболее устойчивую при комнатной температуре α-модификацию серы называют обычно ромбической серой или просто серой.
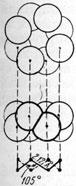
Рис. 77. Вид сверху и сбоку восьмиатомного кольца (молекулы) серы. Ниже дана схема расположения центров атомов
Химический состав. В ряде случаев устанавливается химически чистая сера, но обычно она бывает загряз-нена посторонними механическими примесями: глинистым или органическим веществом, капельками нефти, газами и пр. Известны таже редкие разновидности с изоморфной примесью Se обычно до 1%, изредка до 5,2% - селенистая сера, а также Те, иногда As и в исключительных случаях Тl.
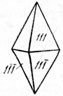
Рис. 78. Кристалл серы пирамидального облика
Сингония ромбическая; ромбо-дипирамидальный в. с. 3L23PC. Кристаллическая структура. Согласно рентгенометрическим исследованиям, ромбическая сера обладает редкой для неорганических соединений молекулярной, и притом очень сложной, решеткой. В кристаллической структуре каждый атом серы с двух сторон имеет сферы, пересекающиеся со сферами соседних атомов, причем цепочки, состоящие из 8 атомов, замкнуты в виде зигзагообразно "сморщенного" кольца (рис. 77). Отсюда видно, что молекула серы S8. Расстояние между атомами S-S равно 2,12 Å. Элементарная ячейка сложена 16 такими электрически нейтральными молекулами (кольцами), очень слабо связанными друг с другом вандерваальсовской связью. Облик кристаллов. Кристаллы чаще имеют пирамидальный (рис. 78) или усеченнопирамидальный вид (рис. 79), реже сфеноэдрический (рис. 80). Характерные формы: {001}, {011}, {111}, {113} и др. Двойники редки - с плоскостью срастания (111), иногда по (011) и (110). Агрегаты. Часто встречается в сплошных, иногда землистых массах. Изредка наблюдаются натечные почковидные формы и налеты (в районах вулканических извержений).
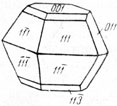
Рис. 79. Кристалл серы усеченнопира-мидального облика
Цвет. У α-серы наблюдаются различные оттенки желтого цвета: соломенно-желтый, медово-желтый, желтовато-серый, бурый и черный (от углеродистых примесей). Черты почти не дает, порошок слабожелтоватый. Блеск на гранях алмазный, в изломе жирный. В кристаллах просвечивает.
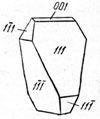
Рис. 80. Сфеноэдрический кристалл серы
Твердость 1-2. Хрупка. Спайность несовершенная по {001}, {110} и {111}. Уд. вес 2,05-2,08. Прочие свойства. Электропроводность и теплопроводность очень слабые (хороший изолятор). При трении заряжается отрицательным электричеством. Растрескивается от теплоты руки.
Диагностические признаки. Характерны цвет, низкая твердость, хрупкость, жирный блеск в изломе кристаллов и легкоплавкость.
П. п. тр. и от спички легко плавится (при 112,8°) и загорается голубым пламенем с выделением характерного запаха SO2 (отличие от похожего на нее аурипигмента - As2S3). Легко растворима в сероуглероде, скипидаре, керосине, но не разлагается в НСl и H2SO4. Крепкая HNO3 и царская водка окисляют серу, переводя ее в H2SO4.
Таким образом, самородная сера, как единственный среди рассматриваемых в этом разделе минерал, обладающий молекулярным строением вещества, характеризуется совершенно особыми свойствами. Наличие - в решетке в качестве структурных единиц электрически нейтральных молекул S8 просто объясняет такие свойства, как плохая электропроводность, низкая теплопроводность, слабая связь между молекулами, что выражается в низких температурах плавления и возгонки, слабых механических свойствах, низкой твердости, в отсутствии ясно выраженной спайности, в связи с чем находятся очень неровный излом и жирный блеск, а кольцевая форма структурных единиц (молекул S8), сильно отличающаяся от формы шара, обусловливает резкую оптическую анизотропию кристаллического вещества, анизотропию теплового расширения и т. д.
Следует добавить, что такие свойства, как небольшой удельный вес и невысокая температура плавления, остроумно используются при добыче самородной серы из глубоко залегающих сероносных пластов: по трубам в буровые скважины нагнетается перегретый водяной пар, и расплавленная сера, освободившись одновременно от посторонних механических примесей, с восходящей струей поднимается на поверхность, где улавливается самыми простыми способами.
Происхождение. Самородная сера встречается исключительно в самой верхней части земной коры и на ее поверхности. Образуется различными путями:
- При вулканических извержениях, осаждаясь в виде возгонов на стенках кратеров, в трещинах пород, иногда изливаясь в жидком виде с горячими водами в виде потоков (Япония). Часто ассоциирует с другими продуктами возгона и сульфатами, образовавшимися при воздействии SO2 на окружающие породы. Возникает в результате неполного окисления сероводорода в сольфатарах или как продукт реакции его с сернистым газом: 2H2S + 20 = 2Н2O + 2S; H2S + SO2 = Н2O + О + 2S.
- При разложении сернистых соединений металлов, главным образом пирита, в нижних частях зоны окисления рудных месторождений. Обычно бывает сильно загрязнена различными механическими примесями.
- При разложении гипсоносных осадочных толщ. Часто наблюдается парагенезис самородной серы с гипсом, на разъеденных участках которого она образуется в виде кристаллических и порошковатых масс. Многое в этом процессе образования еще не ясно.
- Осадочным (биохимическим) путем в нормальных осадочных породах (рис. 57), представленных обычно пластами, содержащими гипс, твердые и жидкие битумы (асфальт, нефть) и др. Этот тип месторождений широко распространен на земном шаре и имеет большое промышленное значение. При этом основная масса самородной серы образовалась, очевидно, сингенетически, т. е. одновременно с другими осадками. Однако нередко наблюдаются и эпигенетические образования серы во вмещающих породах, происшедшие, повидимому, при позднейшей миграции ее под влиянием тектонических процессов, переноса нефтями, растворами и т. п. Происхождение серы биохимическим путем связывают с жизнедеятельностью анаэробных бактерий, в результате чего образуется сероводород, неполное окисление которого приводит к выпадению серы.
Практическое значение. Главное применение сера имеет в производстве серной кислоты, используемой во многих отраслях промышленности; затем в сельском хозяйстве (для борьбы с вредителями), в резиновом производстве (процесс вулканизации резины), при изготовлении спичек, фейерверков, красок и пр.
Месторождения. В СССР широко распространена на территории Средней Азии; следует отметить:
- месторождение Гаурдак;
- Шор-Су - в трещинах и пустотах различных осадочных пород в парагенезисе с нефтью, озокеритом, гипсом, целестином, кальцитом, арагонитом и др.;
- в Каракумской пустыне - в виде бугров, прикрытых кремнистыми корками, в ассоциации с гипсом, квасцами, кварцем, халцедоном, опалом и др. Большие осадочные месторождения имеются в Поволжье (в районе г. Куйбышева) и во многих других местах.
В числе иностранных месторождений большой известностью пользуются крупные месторождения Сицилии, очень мощные месторождения в штатах Тексас и Луизиана (США), связанные с соляными куполами. Интересны по происхождению некоторые месторождения в вулканических районах, образующиеся в виде потоков, застывающих в логах и долинах при излиянии горячих вод с расплавленной серой сольфатарных источников.
|
ПОИСК:
|
© GEOMAN.RU, 2001-2021
При использовании материалов проекта обязательна установка активной ссылки:
http://geoman.ru/ 'Физическая география'
При использовании материалов проекта обязательна установка активной ссылки:
http://geoman.ru/ 'Физическая география'