
Эта неприятная окись азота
Если, как мы говорили, из всех ионосферных областей больше всего хлопот и экспериментаторам, и теоретикам доставила область D, то среди нейтральных частиц первенство по "вредности", несомненно, держит окись азота.
Трудности, возникающие при изучении окиси азота в верхней атмосфере, очень похожи на трудности в постижении природы и поведения области D. Точно так же экспериментальный подход упирается в технические проблемы, а взгляды на теорию претерпевают в течение последних 10 - 15 лет непрерывные изменения, поэтому не удается построить надежных теоретических моделей.
Посмотрим подробнее, в чем же тут дело. Земная атмосфера, как известно, представляет собой смесь в основном азота и кислорода. В такой кислородно-азотной смеси азотные и кислородные частицы, взаимодействуя между собой, неизбежно должны образовывать смешанные продукты - различные окислы азота. Последние обладают большой химической активностью и поэтому вновь легко взаимодействуют с другими атмосферными составляющими- О, O2, N и т. д., что приводит к целой системе сложных фотохимических превращений. Так начинается вся эта "кухня" с окислами азота.
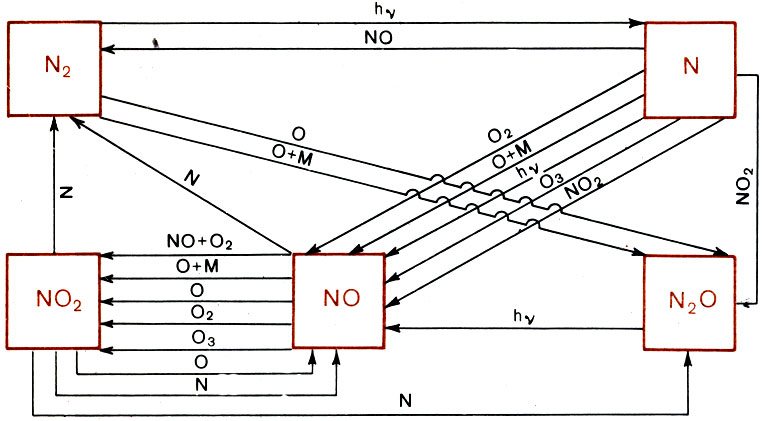
Пути образования NO
Но здесь есть одна тонкость. Молекулярный азот, составляющий большую часть атмосферного газа ниже 100 км, очень инертен. Он ленив, он не хочет вступать ни в какие соединения. Если бы азот на всех высотах в атмосфере существовал только в форме молекул, описанных в этом параграфе, проблем просто не существовало бы, так как не существовало бы практически ни N0, ни других азотных окислов. Но все дело в том, что азот, хотя и слабо, подвержен диссоциации. Молекула N2 под воздействием внешних агентов может распадаться на два атома N, хотя и гораздо менее охотно, чем молекула кислорода. И вот эти порожденные диссоциацией атомы N своей активностью с лихвой компенсируют инертность их родителя - N2. Они готовы взаимодействовать с чем угодно, и с большой эффективностью. Именно они - то и "раскачивают" достаточно инертную систему N2 + O2 и служат инициаторами и активными участниками сложной и разветвленной цепи реакции, в которой замешана интересующая нас окись азота. Действительно, посмотрите на рисунок, на котором представлена примерная схема процессов, происходящих в кислородно-азотной смеси, когда в ней появляется атомный азот. Что и говорить - запутанная картина! Трудно даже понять, что из чего получается, и что во что переходит. Ясно только, что окись азота вовлечена в эту схему очень сильно. И начинать теоретическое изучение распределения N0 надо с процесса диссоциации N2, поскольку атомы N, как мы уже знаем, заваривают всю эту кашу. Но посмотрите вновь на рисунок. Одним из путей образования N0 является реакция О2 с атомами азота
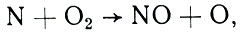
Формула 41
а одним (и весьма важным) из путей гибели - реакция соединения с N
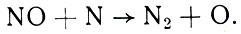
Формула 42
Значит, N и N0 оказываются тесно связанными. Мы рассматриваем здесь только процессы с участием нейтральных частиц. А когда к делу подключатся еще и заряженные частицы, связь между окисью азота и атомным азотом становится еще более тесной и сложной. Мораль проста: невозможно всерьез обсуждать отдельно фотохимию N и N0, приходится говорить о всем цикле процессов с участием азота и его окислов. В этом-то и состоит основная трудность проблемы N0. Решение этой проблемы исторически идет по пути своего рода соревнования между измерениями количества окиси азота и усовершенствованием теории указанного цикла процессов.
Первыми рассмотрели схему реакций с участием N и N0 классики аэрономии англичанин Бейтс и бельгиец Николе. Они получили, что в области D концентрации окиси азота относительно малы и не превосходят 106 молекул на кубический сантиметр. Такой вывод был очень важен, поскольку он показывал, что N0 не может играть существенной роли в образовании области D, Это привело к проблеме дополнительного источника ионизации, описанной в предыдущей главе. Но был ли такой вывод правильным?
Поначалу казалось, что это так. Первое экспериментальное определение количества N0, сделанное японскими учеными, подтвердило выводы теории: количество окиси азота ниже 85 км не превышает 106 см-3.
Здесь следует сделать небольшое отступление - сказать о трудностях измерения N0 в верхней атмосфере. Мы знаем, что основной метод исследования состава атмосферы - масс-спектрометрический. Но окись азота, как бы много внимания ей ни уделяли ученые, является малой составляющей атмосферы. Это означает, что ее концентрации на несколько порядков меньше концентраций основных составляющих атмосферного газа - молекулярного азота и кислорода. Например, на высотах области D, о которых пока в основном ведется наш рассказ, на одну молекулу N0 приходится по меньшей мере 106 (миллион!) частиц N2 и О2. Попробуйте из миллиона частиц выловить одну молекулу N0! Масс-спектрометрам пока это еще не под силу. Да и работают масс-спектрометры ниже 100 км, как мы знаем, весьма неохотно и требуют специальных ухищрений в виде откачных устройств, охлаждения и т. д. Значит, масс-спектрометрический путь определения количества N0 не годится. Нужен метод измерения, позволяющий выделять молекулы окиси азота среди большого количества других частиц. Таким методом в принципе является оптический метод.
Каждая частица (атом или молекула) имеет свой особый спектр поглощения (или излучения), свой "оптический паспорт". Нужно только найти характерные черты этого спектра и произвести измерения в соответствующем интервале длин волн. Эти черты были найдены в виде так называемых γ-полос N0 в ближней ультрафиолетовой части спектра (1800 - 2100 Å). Если аккуратно измерить поглощение атмосферы на различных высотах в указанном интервале длин волн (скажем, с помощью фотометра, поднятого на ракете), то его можно пересчитать в концентрации N0, поскольку именно окись азота служит основным поглощающим агентом в этом интервале λ. Такова идея оптического метода. Но, как обычно, между идеей и ее воплощением стоят серьезные трудности. Они связаны в основном с двумя факторами - калибровкой фотометра и учетом фона рассеянного света, т. е. паразитного сигнала, вызванного излучением, попавшим в прибор помимо поглощающего слоя N0.
Эти экспериментальные трудности и приводят к тому, что к каждому конкретному измерению концентрации N0 приходится относиться с определенной осторожностью. До самого недавнего времени считалось также, что именно с этим связаны в большинстве случаев различия в результатах измерений. Мы вернемся к этому в дальнейшем.
В 1959 году группа японских исследователей опубликовала первые экспериментальные оценки количества N0 в верхней атмосфере. Они использовали весь интервал спектра 1800 - 2100 Å и измеряли суммарную концентрацию окиси азота в столбе атмосферы высотой около 25 км. Эти оценки совпали с теоретическими оценками того времени.
Благополучие это, однако, длилось лет пять. В 1964 году американский ученый Барт опубликовал результаты более тщательных измерений концентраций NO тем же методом. Однако он использовал поглощение в отдельных, более узких полосах и уделил большее внимание вопросу фона рассеянного излучения. Измерения Барта поколебали казавшееся прочным здание фотохимической теории. Согласно его измерениям, количество NO на высотах 75 - 100 км составляет 4×107 см-3, что в 40 раз выше верхнего предела, данного в японской работе. Ситуация резко изменилась. Во-первых, обнаружилось существенное различие между теорией и экспериментом. Во-вторых, стало ясно, что окись азота может играть роль в поддержании ионизации в области D. Как развивалась вторая сторона проблемы, мы уже видели в предыдущей главе. Ну а конфликт между теорией и экспериментом?
Вслед за Бейтсом и Николе многие ученые пытались строить теоретические модели распределения NO на базе схемы фотохимических превращений. И все модели с небольшими вариациями приводили к малым значениям [NO] ниже 100 км, лежащим в пределах 105 - 106 молекул на кубический сантиметр. Надо было искать дополнительный источник окиси азота. Где же его искать? Все варианты комбинаций между N, О и окислами азота в классической схеме тщательно рассмотрены. Требовалась какая-то принципиально новая идея. И такая идея появилась. Ее высказали американские ученые Хантен и МакЭлрой. Что, предположили они, если участвующая в реакции (41) молекула кислорода будет находиться не в обычном, основном, состоянии, а в возбужденном? Скажем, в состоянии О2(1Δg)-наиболее распространенном состоянии возбуждения O2 в верхней атмосфере. Как будет тогда протекать реакция? Есть все основания полагать, что эффективность процесса (41) должна быть на несколько порядков выше, чем в случае невозбужденного кислорода. Но вот на сколько? Покроет ли этот выигрыш в эффективности реакции дефицит в количестве исходных продуктов - ведь возбужденных молекул О2(1Δg) много меньше, чем невозбужденных? Стали считать. Концентрации О2(1Δg) в атмосфере известны (мы поговорим подробнее о возбужденных частицах в конце главы). Значит, можно легко оценить, какая константа скорости реакции
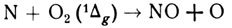
Формула 43
нужна, чтобы обеспечить необходимую скорость образования N0.
Оказалось, что нужно, чтобы величина аз составляла примерно 10-11-10-13см3×с-1 (у разных авторов получались несколько различные оценки из-за неопределенности исходных данных). Эта величина в принципе вполне реальна с точки зрения кинетики реакций, поэтому "вплоть до выяснения" решили, что недостающий механизм генерации окиси азота найден.
Но "выяснение" не замедлило прийти. В лаборатории померили константу реакции (43), и она оказалась равной 3×10-15см3×с-1. На порядки величины ниже, чем необходимо! Новый механизм оказался непригодным для объяснения высоких концентраций окиси азота.
А сами концентрации N0? Не претерпели ли за это время изменений взгляды на их величину? Здесь тоже развернулась бурная дискуссия. Американец Пирс оптическим методом получил [NO]≈109 см3 на высотах области D. Тут уж начался настоящий бум. С одной стороны, нет удовлетворительного механизма, объясняющего даже относительно скромные величины Барта. С другой - возникают совершенно неожиданные сложности с ионизацией в области D. Словом, данные Пирса были признаны завышенными и вину свалили на учет все того же пресловутого фона рассеянного света. Поддержкой такой концепции явился и эксперимент бразильского ученого Мейра. После тщательного учета фона рассеянного света он получил концентрации NO, лежащие между 107 и 108 см-3. Это еще куда ни шло. Во всяком случае, отпали трудности с чудовищными скоростями ионизации на высотах 80-90 км.
Измерения Мейра были признаны наиболее тщательными и на некоторое время приняты в качестве эталона. Правильность их подтверждал и тот факт, что нижний конец кривой Мейра хорошо состыковался с результатами измерений на малых высотах (40 - 65 км) совершенно иным методом.
С данными Мейра стали сравнивать возможности теории. А теория, как мы помним, зашла в тупик в вопросе с реакцией (43), и вновь остро встала проблема источника окиси азота. Пришлось вернуться к исходной реакции (41) между O2 и N. Как повысить ее эффективность? Для невозбужденных О2 и N константа скорости α4 составляет при температуре области D примерно 10-16 см3×с-1. Если возбуждена молекула О2, то эффективность реакции возрастает до 3×10-15 см3×с-1, но этого, как мы видели, недостаточно. А если возбужден атом азота? Такая реакция
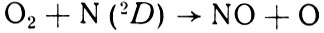
Формула 44
тоже возможна. И, согласно лабораторным данным, идет она довольно эффективно: α4 = 6×10-12 см3×с-1. Но одной эффективности мало. Чтобы оценить вклад этой реакции в образование NО, необходимо знать, какова концентрация исходных продуктов О2 и N (2D) в атмосфере. С О2 проблем нет. А вот возбужденный азот... Его концентрации практически неизвестны. И для высот меньше 100 км не видно даже метода, которым концентрации N(2D) можно было бы измерить. Значит, вновь надежда только на теорию. Теория привела, однако, к парадоксальному выводу: возбужденные атомы N(2D), являющиеся источником окиси азота по реакции (44), образуются в основном из ионов NO+, которые в свою очередь образуются (по крайней мере, на высотах области D) из нейтральных молекул N0. Замкнутый круг!
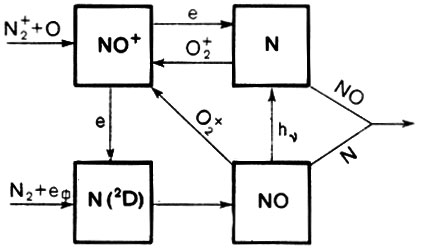
Образование NO
Пришлось включать в рассмотрение и реакции с участием заряженных частиц, что привело к современной схеме процессов, включающей как N, N(2D) и N0, так и положительные ионы. Эта схема изображена на рисунке. Мы видим, что все интересующие нас компоненты в этой схеме взаимосвязаны. Чтобы найти нужные нам концентрации отдельных составляющих, приходится решать довольно громоздкую систему уравнений, вытекающую из указанной схемы. Задача сложная, но вполне разрешимая.
Соответствующие расчеты были сделаны, и они показали, что теория на данном этапе хорошо согласуется с результатами эксперимента Мейра. Более того, выше 140 км удалось измерить концентрации возбужденных атомов N(2D) оптическим методом. И по этому параметру теория и эксперимент оказались в хорошем согласии. Остается еще третья интересующая нас в этой главе компонента - атомный азот N в основном состоянии. Но по нему, как мы увидим далее, пока нет надежных экспериментальных данных, значит, и говорить о контроле теории экспериментом пока нельзя.
Каково же на сегодняшний день положение с теорией и измерениями окиси азота?
Фотохимию N0 мы уже обсудили. Пока это лучшее, что есть. Но уже видны некоторые подводные камни. Например, роль реакции
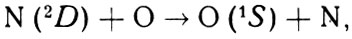
Формула 45
передающей возбуждение от атомов азота к атомам кислорода.
Насколько она эффективна? Ведь в описанной выше схеме считается, что все образующиеся атомы N(2D) превращаются в N0 по реакции (44). Но если реакция с О идет достаточно быстро, часть атомов N(2D) будет "утекать" из канала образования N0 и наша схема опять нарушится - будет вновь не хватать мощности источника образования окиси азота. Вопрос, таким образом, упирается в эффективность реакции (45), но эта эффективность, увы, пока неизвестна.
Что касается экспериментальных данных, то здесь появилось много интересного. Американским ученым со спутника удалось провести многочисленные и, видимо, надежные оптические измерения распределения окиси азота с высотой выше области Е.
Одним из важных выводов, полученных в результате измерений, является вывод о том, что существуют небольшие, но хорошо выраженные широтные вариации концентрации N0. В полярной области [NO] оказались систематически в 2 - 3 раза выше, чем в средних широтах. Вывод этот существен по двум причинам. Во-первых, он - свидетельство пространственной изменчивости NO. В совокупности с косвенными оценками, о которых мы поговорим ниже, это заставляет рассматривать окись азота как очень динамичную компоненту. Во-вторых, он ставит под сомнение результат, полученный несколько лет назад. На ракетах во время полярного сияния были измерены огромные концентрации N0 в области Е ([NO] оказалась примерно равна [О2], что в 105 раз больше, чем в средних широтах!). Предполагалось, что столь высокие [NO] обязаны своим происхождением очень эффективному образованию атомов N(2D) вторгающимися потоками частиц. Но частицы (и в первую очередь электроны) вторгаются в полярную ионосферу довольно регулярно. И тем не менее измерения на спутнике ничего сравнимого с ракетным экспериментом не обнаружили. Пришелся ли этот эксперимент на уникальные условия или он был ошибочным? Пока нельзя сказать окончательно, но с точки зрения наших сегодняшних знаний вероятнее второе.
Итак, выше области Е мы теперь имеем целый набор измерений количества окиси азота. А в самой области Е и ниже? Про прямые измерения NO оптическим методом на этих высотах мы уже говорили. Но в последнее время появилось много косвенных оценок [NO] в Е- и D-области. И эти оценки заставили по-новому взглянуть на проблему экспериментальных определений [NO] в целом. Выше мы видели, как активно окись азота вмешивается в вопросы ионизации, рекомбинации и образования ионов-связок. А раз так - любые вариации количества NO должны находить отражение в поведении различных ионосферных параметров. Простейший пример: отношение двух основных молекулярных ионов NO+ и О2+ на высотах 85 - 120 км. Оно прямо зависит от концентрации окиси азота, которая превращает O2+ в NO+:
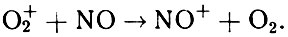
Формула 46
Значит, анализ отношения [NO+]/[O2+], которое получается во всех экспериментах по измерению ионного состава, может дать столь нужные нам сведения о количестве и вариациях [NO].
Ниже 85 км все обстоит несколько сложнее из-за уже известных нам трудностей ионной химии области D. Но и здесь удается проследить за поведением NO на основании измерений концентрации заряженных частиц.
Что же дали все эти косвенные оценки? Совершенно неожиданный результат: окись азота - очень изменчивая компонента атмосферы. В области Е уже обнаружены суточные, сезонные и связанные с солнечной активностью вариации [NO]. В области D получены широтные вариации и вариации с солнечной активностью, а также сильные изменения [NO] во время явлений зимней аномалии и стратосферных потеплений. При этом в ряде случаев амплитуда вариаций может быть очень велика. Например, во время явления зимней аномалии получены концентрации N0 порядка 109 см3×с-1, что на полтора порядка выше, чем в невозмущенных условиях.
Из факта существования таких сильных вариаций концентраций NО в области Е и особенно в области D непосредственно следуют два вывода. Первый вывод: необходимо пересмотреть подход к экспериментальным определениям [NO]. Действительно, вправе ли мы теперь ожидать согласия (близкого совпадения измеряемых концентраций) между различными экспериментами? Очевидно, нет. Если концентрации NO столь изменчивы, различие в результатах может свидетельствовать лишь о разных условиях проведения экспериментов, а не о неточности одного из измерений. Такой подход легко объясняет часть противоречий, рассмотренных выше и приписанных трудностям калибровки, учета фона рассеянного излучения и т. д. Второй вывод касается процессов, контролирующих распределение [NO]. Фотохимию окиси азота мы обсудили выше. Но могут ли только фотохимические процессы обеспечить такую сильную изменчивость концентрации NО? Сегодня мы отвечаем на этот вопрос отрицательно. Стало быть, надо рассмотреть возможности других процессов - динамических.
На концентрации нейтральных частиц в верхней атмосфере могут влиять три типа процессов: молекулярная диффузия, турбулентная диффузия и горизонтальный перенос. Роль каждого из этих процессов определяется временем жизни данных частиц М относительно соответствующего процесса. Относительно какого процесса время жизни меньше, тот и определяет на данных высотах распределение [М]. В случае N0 мы можем довольно аккуратно сравнить времена жизни относительно молекулярной диффузии и фотохимии. Они оказываются равными на высоте около 200 км. Выше доминирует молекулярная диффузия, которая и определяет вертикальный профиль [NO]. Ниже - фотохимия. До каких пор? Пока ее не "переможет" турбулентная диффузия. Но сделать точные оценки этой высоты труднее, поскольку все еще нет надежных данных о коэффициенте турбулентной диффузии, а он-то как раз и определяет необходимое нам время жизни. Можно лишь утверждать, что в области D концентрации окиси азота контролируются именно турбулентной диффузией, которая вместе с фотохимией контролирует, видимо, профиль [N0] и в нижней части области Е.
Помогает ли все это объяснить сильную изменчивость [NO] в областях D и Е? Видимо, нет. Правда, неопределенность с коэффициентом турбулентной диффузии оставляет некоторые возможности для объяснения изменчивости [NO] вариациями этого коэффициента, но в целом в настоящее время считается неизбежным привлекать для объяснения этой изменчивости процессы горизонтального переноса. Увы, дальше этого дело пока не идет. Мы не знаем ни эффективности процесса, ни причины его изменчивости, ни места, откуда, скажем, поступают молекулы N0, создающие высокие концентрации в тех или иных условиях. Вопросов, подобных этим, много. Однако пристальное внимание к проблеме вариаций окиси азота в нижней ионосфере обещает в ближайшее время ответы (и, возможно, очень интересные) по крайней мере на некоторые из них.
|
ПОИСК:
|
© GEOMAN.RU, 2001-2021
При использовании материалов проекта обязательна установка активной ссылки:
http://geoman.ru/ 'Физическая география'
При использовании материалов проекта обязательна установка активной ссылки:
http://geoman.ru/ 'Физическая география'