
1. Группа барита
Сюда относятся сернокислые соединения Sr, Ba и Рb, не встречающиеся в природе в виде водных сульфатов. Безводный сульфат кальция (ангидрит) хотя кристаллизуется в той же ромбической сингонии, что и указанные сульфаты, но существенно отличается от них как по кристаллической структуре, так и по формам кристаллов, что связано с меньшей величиной радиуса иона Са2+. Так как ангидрит по условиям образования в природе чрезвычайно тесно связан с водным сульфатом кальция (гипсом), то подробную характеристику его мы дадим отдельно, вместе с гипсом.
Барит - BaSO4. "Барос" по-гречески - тяжесть. Большой удельный вес этого минерала легко ощутим в руке. Среди очень немногочисленных бариевых минералов барит является главным, а среди безводных сульфатов - наиболее распространенным после ангидрита.
Химический состав. ВаО 65,7%, SO3 34,3%. В виде изоморфных примесей устанавливаются Sr и Са. Разновидность с высоким содержанием стронция называется баритоцелестином. Изредка встречаются разности, богатые Рb и Ra (хокутолит). Из посторонних примесей устанавливаются иногда Fe2O3, глинистые, органические и прочие вещества.
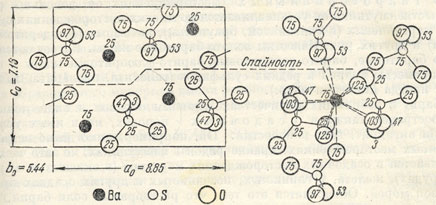
Рис. 232. Кристаллическая структура барита в проекции вдоль оси b
Сингония ромбическая; ромбо-дипирамидальный в. с. 3L23PC. Кристаллическая структура. На рис 232 показана проекция элементарной ячейки структуры вдоль осп 6, перпендикулярной к плоскости чертежа. Ионы Ва2+ и S6+ располагаются на расстояниях в 1/4 и 3/4 высоты b (см. цифры). Группы SO4, как можно видеть по цифрам, ориентированы таким образом, что два кислородных иона лежат горизонтально, а два других - вкрест по отношению к первым. Каждый ион Ва окружен 12 кислородными ионами, принадлежащими к семи различным группам SO4 (рис. 232 справа). Облик кристаллов. Часто встречающиеся кристаллы барита обычно обладают таблитчатым обликом (рис. 233) вследствие развития граней {010} (в установке Е. С. Федорова). Реже распространены призматические, столбчатые (рис. 233), обычно образованные господствующими гранями призм {011} или {110} в комбинации с {010}, и изометрические кристаллы. Часто чрезвычайно богаты комбинациями. Двойники не часты по (201), (О11); обычно наблюдаются полисинтетические двойники, обусловливающие штриховатость на гранях. Агрегаты чаще зернистые, реже плотные, скрытокристаллические, землистые. Наблюдаются также в виде сталактитов и других натечных форм с концентрически-зональным строением. Известны шаровидные и эллипсоидальные конкреции с радиальнолучистым строением. В пустотах часто удается наблюдать эффектные друзы небольших кристаллов.
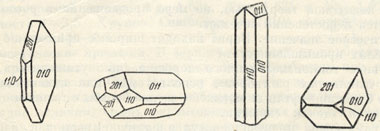
Рис. 233. Кристаллы барита
Цвет. Встречаются бесцветные водяно-прозрачные кристаллы. Большей же частью барит посторонними примесями окрашен в белый или серый (микроскопическими включениями газов и жидкостей), красный (окисью железа), желтый или бурый (вероятно гидроокислами железа), темносерый и черный (битуминозными веществами), иногда голубоватый, зеленоватый и другие оттенки. Блеск стеклянный, на плоскостях спайности {010} перламутровый. Ng = 1,648, Nm = 1,637 и Np = 1,636.
Твердость 3-3,5. Хрупок. Спайность по {010} совершенная, по {201} средняя и по {001} несовершенная. Уд. вес 4,3-4,7.
Диагностические признаки. Среди наиболее широко распространенных сульфатов барит обладает самым большим удельным весом (лишь у англезита уд. вес выше). Характерны совершенная спайность в одном направлении, нерастворимость в НCl даже при нагревании (отличие от всех карбонатов). От некоторых силикатов, похожих на него по спайности и другим признакам, отличается значительно меньшей твердостью. Без химических реакций трудно отличим от целестина.
П. п. тр. растрескивается, сплавляется лишь в тонких осколках по краям, причем пламя окрашивается в желто-зеленый цвет (характерно для бария). С содой на платиновой пластинке сплавляется в прозрачную массу, которая по охлаждении становится мутной (при сплавлении на угле эта масса расплывается и впитывается внутрь). В отличие от целестина, сернистый барий, получающийся в восстановительном пламени п. п. тр., после смачивания НСl окрашивает пламя не в карминно-красный, а в желто-зеленый цвет. В концентрированной H2S04 в порошкообразном состоянии медленно растворяется. От прибавления воды раствор мутнеет, т. е. снова выделяется BaSO4.
Происхождение. Барит в природе образуется различными путями, но лишь в условиях повышенного парциального давления кислорода и при относительно низких температурах. Поэтому он, подобно всем другим безводным сульфатам, не встречается как магматогенный минерал в изверженных, а также в глубинных метаморфических породах.
В гидротермальных месторождениях он довольно обычен. В качестве спутника он устанавливается во многих месторождениях сульфидных, марганцевых (с манганитом, браунитом), железных (с сидеритом, гематитом) и других руд. Известны золото-баритовые жилы. Встречаются почти чисто баритовые, барито-кальцитовые, барито-флюоритовые жилы с небольшой примесью кварца и редких сульфидов (галенита, сфалерита, халькопирита, иногда киновари и др.).
Барит в небольших количествах, главным образом в виде конкреций, распространен также в осадочных породах, но в иных условиях, нежели ангидрит, гипс и целестин. Он, например, никогда не встречается в соляных месторождениях, крайне редок в известняках, но зато часто устанавливается в осадочных месторождениях марганца (в окисных и карбонатных рудах), железа, в глинистых, песчанистых и других осадках прибрежных зон морей. Объясняется это тем, что растворимые соли бария, приносимые с суши поверхностными водами, при первой же встрече с ионами |SO4]2- в морских водах образуют практически нерастворимый сульфат бария. Желваки барита обнаруживаются среди илов и в современных морях.
В зонах выветривания горных пород и рудных месторождений в районах с сухим климатом при внимательном изучении мелкие кристаллы барита часто столбчатого облика нередко устанавливаются в ассоциации с гипсом и гидроокислами железа.
Барит - химически устойчивый минерал, поэтому устанавливается в элювии, нередко в крупных обломках, а также в шлихах, получаемых при промывке россыпей. Однако, как все минералы, обладающие хорошей спайностью и невысокой твердостью, по мере продвижения в россыпи быстро измельчается и постепенно исчезает.
Практическое значение. Барит находит широкое применение в различных отраслях промышленности.
- В виде тонкоизмельченного порошка, как утяжелитель, вводится в состав "глинистых растворов", используемых для цементации рыхлых пород при бурении нефтяных залежей с целью борьбы с газовыми выбросами и укрепления стенок скважин.
- В химической промышленности является сырьем для изготовления различных солей и препаратов, используемых в пиротехнике, кожевенном деле (для удаления волос), сахарном производстве, при изготовлении фотобумаги, в керамике для производства эмалей, для выплавки специальных стекол, обладающих высоким коэфициентом преломления, в медицине и т. д.
- В резиновой и бумажной промышленности применяется в качестве наполнителя и утяжелителя.
- В лако-красочной промышленности употребляется для производства высокосортных белил (в смеси с ZnO и ZnS), цветных красок и др.
- Как главная составная часть штукатурки для стен рентгеновских лабораторий употребляется с целью защиты работников от вредного действия рентгеновских лучей.
- Металлический барий применяется для изготовления некоторых радиоламп.
Месторождения. Из многочисленных месторождений барита в СССР укажем лишь главнейшие. В Западной Грузии имеется ряд жильных баритовых месторождений в Кутаисском, Болнисском и других районах, среди туфов и эффузивных пород (порфиритов). Сплошные баритовые массы симметричнополосчатого или колломорфного строения в виде примесей содержат: кальцит, в очень небольшом количестве кварц, изредка пирит, халькопирит и галенит. Месторождения Каракалинского района в Туркменской ССР (в горах Копетдага) также представлены целой серией жил в осадочных породах (песчаниках, глинистых сланцах и др.). В ряде жил (Арпаклен) барит находится в ассоциации с витеритом (ВаСO3), который местами псевдоморфно развивается по бариту.
К числу крупнейших иностранных месторождений барита принадлежит Мегген в Вестфалии (Германия). Здесь огромной длины (до 7 км) пластообразная залежь, местами сопровождающаяся залежью сульфидов, главным образом пирита, располагается на границе между средне- и верхнедевонскими осадками. Происхождение этой залежи точно не выяснено.
Целестин - SrSO4. "Целестис" по-латыни - небесный (первые найденные образцы этого минерала имели нежноголубой оттенок). Относительно редко встречается, но среди минералов стронция он является главным.
Химический состав. SrO 56,4%, SO3 43,6%. Иногда содержит Са и Ва (нередко в значительных количествах).
Сингония ромбическая; ромбо-дипирамидальный в. с. 3L23PC.
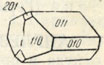
Рис. 234. Кристалл целестина (установка E.С. Федорова)
Кристаллическая структура совершенно аналогична структуре барита. Облик кристаллов. Встречающиеся кристаллы очень похожи на кристаллы барита. Обычно имеют таблитчатый, столбчатый или призматический (рис. 234) облик. Агрегаты чаще зернистые, реже шестоватые, жилковатые и скорлуповатые с общей натечной формой. Встречается в виде желваков и секреций, причем в пустотах наблюдаются друзы кристаллов.
Цвет целестина голубовато-белый или голубовато-серый, реже с красноватым или желтоватым оттенком. Иногда обнаруживаются бесцветные, водяно-прозрачные кристаллы. Блеск стеклянный, на плоскостях спайности-перламутровый отлив. Ng=l,631, Nm = l,624 и Np = 1,622.
Твердость 3-3,5. Хрупок. Спайность по {010} совершенная, по {201} средняя. Уд. вес 3,9-4,0.
Диагностические признаки. В зернистых массах от карбонатов Mg, Са, Sr, Ва и др. отличим по поведению в кислотах (карбонаты при растворении с нагреванием выделяют СO2). По цвету иногда похож на ангидрит, но отличается по направлениям спайности и большему удельному весу. От барита часто трудно отличим. Очень характерна реакция на стронций.
П. п. тр. плавится в белый шарик, окрашивая пламя в интенсивный карминно-красный цвет, особенно после смачивания НСl (реакция на стронций). На угле с содой дает серную печень. В крепкой H2SO4 растворяется. Раствор мутится при прибавлении воды.
Происхождение. Целестин в более или менее значительных массах в виде желваков, гнезд, иногда сплошных залежей встречается в толщах осадочных пород (в доломитах, известняках, гипсоносных глинах, мергелях и др.). Его находки нередко бывают приурочены к определенным горизонтам среди этих пород.
Он был также установлен в морских организмах, в частности в скелете одной группы радиолярий. Иногда он встречается в раковинах аммонитов и в других окаменелостях, по всей вероятности как результат позднейшего отложения в них.
Известны, правда очень редкие, но типичные гидротермальные жилы целестина, содержащие галенит, сфалерит и другие сульфиды. Наблюдался также в миндалинах изверженных пород.
Практическое значение. Целестин является главным источником солей стронция, употребляемых в пиротехнике (для получения яркого карминно красного пламени) и в химической промышленности: сахарной (в виде окиси стронция для удаления сахара из меломассы), стекольной и керамической (для изготовления иризирующих стекол, особых глазурованных кирпичей) и пр. В последнее время начали применять стронций в виде металла при производстве специальных сплавов, например в качестве присадки к меди с целью повышения ее прочности и однородности (электропроводность при этом не снижается).
Месторождения. Целестин довольно часто встречается в виде секреций в осадочных гипсоносных породах пермского возраста, распространенных в Архангельской области, в Верхнем и Среднем Поволжье, Башкирии, Чкаловской области и др. Значительное количество пунктов нахождения известно также в Закаспии (в Туркмении, па о. Мангышлак и др.) и других районах СССР.
Из иностранных месторождений отметим крупные месторождения целестина в районах Бристоля (Англия), Вестфалии и Вальдека (Германия).
Англезит - PbSO4. Впервые был установлен на о. Англези (Уэлс), откуда и произошло его название.
Химический состав. РbО 73,6% (Рb 68,3%), SO3 26,4%. От примесей обычно свободен. Известна разность, богатая ВаО (8,45%).
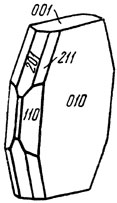
Рис. 235. Кристалл англезита
Сингония ромбическая; ромбо-дипирамидальный в. с. 3L23PC. Кристаллическая структура совершенно аналогична структуре барита. Облик кристаллов. Кристаллы англезита часто весьма богаты комбинациями граней. Обычно имеют таблитчатый облик (рис. 235), реже короткостолбчатый или пирамидальный. Крупные кристаллы вообще редки. Агрегаты. Чаще встречается в виде кристаллических корочек на галените, друз мелких кристаллов, в плотных зернистых или землистых массах.
Цвет. Бесцветен и часто водяно-прозрачен. Нередко окрашен в белый, серый, желтоватый или бурый цвет (гидроокислами железа). Наблюдающийся иногда черный цвет обусловлен микроскопическими включениями неразложившегося галенита. Блеск алмазный. Ng = 1,894, Nm=1,882 и Np = 1,877.
Твердость 2,5-3. Весьма хрупок. Спайность несовершенная по {010} и {210}. Уд. вес 6,1-6,4. Диагностические признаки. Для англезита характерны высокий удельный вес, алмазный блеск, в окисленных рудах тесная ассоциация с галенитом и поведение перед паяльной трубкой.
П. п. тр. растрескивается и легко плавится. На угле с содой дает серную печень и затем в восстановительном пламени-королек свинца. В концентрированной H2SO4 растворяется лишь при нагревании. Однако полностью растворяется в КОН (отличие от целестина и барита).
Происхождение. Как труднорастворимый продукт окисления галенита и других сернистых соединений свинца англезит образуется главным образом в зонах окисления свинцово-цинковых сульфидных месторождений, очень часто в ассоциации с гораздо более распространенным церусситом (РbСO3).
Как показывает изучение под микроскопом, англезит является первым кислородным соединением свинца, которое возникает при окислении галенита по периферии и вдоль направлений спайности по реакции: PbS + O4=PbSO4. Однако англезит под влиянием углекислоты в свою очередь легко переходит в карбонат свинца - церуссит (РbСO3). Оба эти минерала в силу низкой их растворимости в воде обычно образуют вокруг кусков сплошного галенита белую корку, предохраняющую от дальнейшего окисления центральные участки галенита*. Этим объясняется тот факт, что при разбивании округлых белых желваков, казалось бы, нацело окисленных свинцовых руд в центральных частях нередко обнаруживается сплошной галенит. Дальнейшее окисание галенита может происходить лишь по мере превращения англезита в карбонат свинца.
*(На этом свойстве основано хранение серной кислоты в сосудах, внутренние стенки которых покрыты слоем металлического свинца: образующаяся нерастворимая тонкая оболочка PbSO4 столь плотна, что не допускает дальнейшего превращения свинца в сульфат)
Характерно также, что общее содержание свинца в зонах окисления всегда выше, чем в первичных сульфидных рудах. Это обусловлено тем, что постоянный спутник галенита-сфалерит и сульфиды меди при окислении переходят в легкорастворимые сульфаты и выносятся, за счет чего и происходит обогащение окисленных руд свинцом.
Англезит может образоваться и гидротермальным путем, правда в особых условиях. В виде прекрасно образованных, часто довольно крупных кристаллов он встречается в таких свинцово-цинковых месторождениях, отложение руд которых, судя по парагенезису минералов и формам минеральных агрегатов, могло происходить вблизи дневной поверхности (вероятно при смешении с вадозовыми насыщенными свободным кислородом подами). Таковы, например, месторождения Райбл и Блейберг в Каринтии (Восточные Альпы), где кристаллы англезита в пустотах встречаются наряду с нетронутыми окислением сульфидами Fe, Zn и Pb.
Практическое значение. При разработке зон окисления свинцовых месторождений англезит вместе с другими кислородными соединениями свинца идет в плавку.
Месторождения. В тех или иных количествах англезит всегда удается установить в зонах окисления всех галенитсодержащих сульфидных месторождений. Останавливаться на перечислении их не будем. Укажем лишь, что в нашей литературе описаны хорошо образованные кристаллы из месторождений: Березовского золоторудного (Урал), ряда алтайских, Нерчинских (Восточное Забайкалье) и др.
| Наименование минерала | Твердость | Уд.вес | Цвет | Блеск | Ng | Nm | Np |
|---|---|---|---|---|---|---|---|
| Ангидрит - CaSO4 | 3-3,5 | 2,9 | Белый | Стеклянный | 1,614 | 1,576 | 1,571 |
| Целестин - SrSO4 | 3-3,5 | 3,9 | Голубой | >> | 1,631 | 1,624 | 1,622 |
| Барит - BaSO4 | 3-3,5 | 4,5 | Белый | >> | 1,648 | 1,637 | 1,636 |
| Англезит - PbSO4 | 2,5-3 | 6,3 | >> | Алмазный | 1,894 | 1,882 | 1,877 |
Обобщение. Подведем итог главнейшим отличительным свойствам минералов группы барита, включая сюда и ангидрит. Как можно видеть из данных табл. 10, сульфат свинца сильно отличается по своим свойствам от других аналогичных сульфатов металлов. Он существенно отличен и по условиям образования в природе. Сульфаты Са, Sr и Ва друг от друга заметно отличаются по удельному весу и коэфициентам преломления.
|
ПОИСК:
|
© GEOMAN.RU, 2001-2021
При использовании материалов проекта обязательна установка активной ссылки:
http://geoman.ru/ 'Физическая география'
При использовании материалов проекта обязательна установка активной ссылки:
http://geoman.ru/ 'Физическая география'