
3. Группа сфалерита
Сюда относятся диморфные минералы типа АХ, кристаллизующиеся в кубической и гексагональной сингониях (в кристаллических структурах типа сфалерита и вюртцита с тетраэдрической координацией ионов). Здесь же рассмотрим сульфид ртути (киноварь), хотя и близкий по некоторым свойствам к группе сфалерита, но существенно отличающийся по кристаллической структуре.
Сфалерит - ZnS. Название происходит от греческого слова "сфалерос" - обманчивый, очевидно, потому, что по внешним признакам он совершенно непохож на обычные сульфиды металлов. Синоним: цинковая обманка.
Разновидности:
- клейофан - светлоокрашенная или бесцветная разновидность (почти без примесей);
- марматит - черная железистая разновидность сфалерита;
- пршибрамит - богатая кадмием (Cd до 5%) разновидность (Zn, Cd) S.
Химический состав. Zn 67,1%, S32,9%. В качестве примесей чаще всего присутствует Fe (до 20%); такие разновидности под микроскопом обнаруживают мельчайшие включения пирротина (FeS) как продукта распада твердого раствора. Иногда в виде таких же включений присутствует халькопирит (CuFeS2) и изредка станнин (Cu2FeSnS4), чем объясняется примесь в сфалерите меди и олова. Нередко в виде изоморфной примеси присутствуют: Cd (обычно до десятых долей процента), In (до сотых долей процента), Ga, Mn, Hg и др.
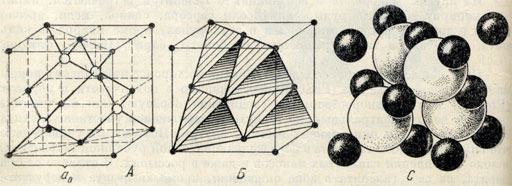
Рис. 94. Кристаллическая структура сфалерита. А - расположение центров ионов цинка (черные кружочки) и серы (светлые кружочки); Б - та же решетка, изображенная в виде тетраэдров, внутри каждого из которых располагаются центры ионов серы, С - кристаллическая структура, изображенная в виде шаров
Сингония кубическая; гексатетраэдрический в. с. 3L424L36P. Кристаллическая структура похожа на структуру алмаза, с той разницей, что центры малых кубов заняты иными атомами (ионами), чем вершины и центры граней большого куба. Как показано на рис. 94, вокруг каждого иона S по вершинам тетраэдра располагаются четыре иона цинка. В элементарной ячейке, показанной на этих рисунках, заключено четыре иона серы, занимающие центры половинного числа малых кубов. Характерно, что все эти тетраэдры ориентированы одинаково, что и приводит в целом к симметрии тетраэдра, а не куба. В отличие от алмаза, спайность в кристаллах сфалерита проходит не по плоскостям октаэдра, а по плоскостям ромбического додекаэдра {110}, так как эти плоские решетки одновременно содержат ионы Zn и S, и притом в равных количествах.
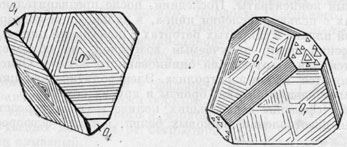
Рис. 95. Тетраэдрические кристаллы сфалерита
Облик кристаллов. Часто встречается в виде хорошо образованных кристаллов в друзовых пустотах. Облик чаще всего тетраэдрический (рис. 95), причем положительные и отрицательные формы нередко отличаются характером блеска и фигурами травления. Двойники не редки по {111}. Агрегаты. Сплошные массы характеризуются явнозернистой структурой, легко распознаваемой благодаря резко проявленной спайности в отдельных зернах. Реже встречаются почковидные формы образований.
Цвет сфалерита обычно бурый или коричневый; часто черной (марматит), реже желтой, красной и зеленоватой окраски. Известны совершенно бесцветные прозрачные разности (клейофан). Черта белая или светло окрашенная в желтые и бурые оттенки. Разности, богатые железом, дают коричневую черту. Блеск алмазный. Показатель преломления в Na-свете N = 2,37.
Твердость 3-4. Довольно хрупок. Спайность весьма совершенная по {110}. Уд. вес 3,5-4. Прочие свойства. Электричества не проводит. Обладает полярным термоэлектричеством. Некоторые разновидности при трении или раскалывании фосфоресцируют.
Диагностические признаки. Характерны изометрической формы кристаллические зерна, обладающие спайностью по ромбическому додекаэдру, т. е. по шести направлениям, отвечающим плоским сеткам в решетке, сложенным атомами цинка и серы. Этим железистые разности сфалерита легко отличаются от весьма похожих на них по цвету, твердости, блеску и другим признакам вольфрамита - (Fe,Mn)WO4 и энаргита - Cu3AsS4, которые обладают призматическим обликом зерен и спайностью в одном направлении.
П. п. тр. растрескивается, но почти не плавится. В окислительном пламени на угле дает белый налет окиси цинка. В концентрированной HNO3 растворяется с выделением серы.
Происхождение. Главная масса месторождений сфалерита, так же как и галенита, с которым он почти постоянно ассоциирует, принадлежит к гидротермальным месторождениям (см. галенит). В некоторых сульфидных месторождениях он парагенетически бывает связан с халькопиритом.
В экзогенных условиях образуется крайне редко. Он был встречен в некоторых осадочных месторождениях угля.
При процессах окисления сфалерит разлагается сравнительно быстро с образованием сульфата цинка, легко растворимого в воде, вследствие чего зоны окисления бывают сильно обеднены цинком (ср. галенит). Если боковые породы месторождения представлены известняками, то в них образуются скопления карбоната цинка - смитсонита.
Практическое значение. Сфалерит является главной рудой цинка. Попутно с цинком из сфалеритовых руд извлекаются ценные редкие металлы: Cd, In и Ga.
При обжиге и плавке полиметаллических руд ZnS, окисляясь в ZnO, в значительной мере улетучивается с отходящими газами. Поэтому обычно прибегают к предварительному обогащению руд с разделением их на свинцовый и цинковый концентраты. Последний, после предварительного обжига в особых печах с целью окисления цинка, в дальнейшем подвергается восстановительной плавке в закрытых ретортах с перегонкой цинка.
Металлический цинк, получаемый возгонкой, не обладает чистотой и употребляется для изготовления оцинкованного железа. Очистка сырого цинка производится путем электролиза. Электролитический цинк употребляется для изготовления латуни, бронзы и других сплавов.
Кроме того, сфалерит в небольших количествах непосредственно употребляется для изготовления цинковых белил, а также флюоресцирующих экранов и др.
Кадмий, в главной своей массе добываемый попутно из сфалеритовых руд, находит применение: в гальванопластике при покрытии изделий из стали и железа с целью борьбы с коррозией металла; для получения легкоплавких сплавов, более прочных и обладающих большей сопротивляемостью высоким температурам и истиранию, чем баббитовые, в состав которых в значительном количестве входит дефицитное олово в производстве аккумуляторов; для автоматических противопожарных аппаратов и др.
Галлий представляет собой металл, по свойствам во многом напоминающий алюминий; он плавится при 29°, а с алюминием образует сплав, при обыкновенной температуре жидкий; температура кипения галлия, в отличие от ртути, очень высокая (1700-2300°), что позволяет его применять в ряде случаев вместо ртути для наполнения термометров и других точных приборов. Галлиевые лампы дают свет, близкий к солнечному.
Индий как антикоррозионный металл употребляется для покрытий металлических изделий, а также в производстве рефлекторов для прожекторов и автомобильных фар. Органические соединения индия применяются для борьбы с сонной болезнью.
Месторождения. Сфалерит в свинцово-цинковых месторождениях, отдельные примеры которых были приведены выше (см. галенит), как правило, значительно преобладает в количественном отношении над галенитом.
В некоторых месторождениях встречаются друзы хорошо образованных кристаллов сфалерита с кальцитом, кварцем и другими минералами, например в месторождениях Нагольного кряжа (Украина) и в других.
В ряде пунктов встречены очень интересные метаколлоидные образования сфалерита в виде концентрически-полосчатых почковидных выделений в известняках в ассоциации с галенитом, пиритом, марказитом, халькопиритом, кальцитом или доломитом.
В тесной ассоциации с халькопиритом (почти без галенита) наблюдается в ряде так называемых колчеданных залежей Урала: месторождения Карпушинское, им. III Интернационала и др.
Из наиболее интересных в минералогическом отношении иностранных месторождений отметим следующие: Пршибрам (Чехословакия); прекрасные кристаллы в пустотах среди доломита в Биннентале (Швейцария), замечательные по прозрачности кристаллы сфалерита из месторождений района Сантандер (Северная Испания).
Вюртцит - ZnS. Разновидность: эритроцинкит - марганецсодержащий вюртцит (Zn,Mn)S.
Химический состав такой же, как у сфалерита. Обычно содержит повышенное количество кадмия.
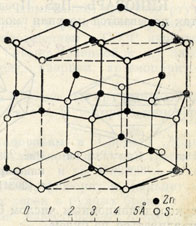
Рис. 96. Кристаллическая решетка вюртцита
Сингония гексагональная; дигексагонально-пирамидальный в. с. L66P. Кристаллическая структура почти тождественна структуре сфалерита. В обеих модификациях ZnS каждый ион S лежит между четырьмя ионами Zn. Структура вюртцита легко может быть выведена из структуры сфалерита, если решетку сфалерита изобразить стоящей на грани тетраэдра. В слоях ионов, параллельных {0001}, ионы цинка, как видно на рис. 96, располагаются несколько выше ионов серы. Близость кристаллических решеток сфалерита и вюртцита сказывается и в близости ряда их физических свойств: цвета, прозрачности, показателей преломления, твердости, удельного веса и др. Облик кристаллов пирамидальный, короткостолбчатый или таблитчатый. Агрегаты. Нередко встречается в метаколлоидных массах с радиальноволокнистым строением.
Цвет вюртцита, так же как и у сфалерита, варьирует, в зависимости главным образом от примеси Fe, от светлого до бурого и черного. Черта соответственно меняется от бесцветной до бурой. Блеск алмазный.
Твердость 3,5-4. Хрупок. Спайность совершенная по {1120} и несовершенная по {0001}. Уд. вес 4,0-4,3.
Диагностические признаки. В сплошных массах внешне не отличим от сфалерита. Оптическая анизотропия его может быть установлена только под микроскопом. По поведению перед паяльной трубкой и в кислотах не отличим от сфалерита.
Происхождение. Является сравнительно редким минералом. В некоторых гидротермальных месторождениях, образовавшихся при низких температурах, встречается совместно со сфалеритом.
Месторождения. В очень незначительных количествах совместно со сфалеритом установлен в некоторых месторождениях Урала: Блява, Яман-Касы; на территории Киргизской ССР: Ак-Тюз, Караваш и др.
Из иностранных месторождений наибольший минералогический интерес представляют следующие: концентрически-зональные метаколлоидные разности в Пршибраме (Чехословакия), хорошо образованные пирамидальные кристаллы месторождений Бьютт в Монтане (США), Оруро и Потози (Боливия) и др.
Самостоятельного практического значения этот минерал не имеет.
Гринокит - CdS. Синоним: кадмиевая обманка. Редкий. Содержание Cd 77%. Иногда содержит индий.
Сингония гексагональная. Редко встречающиеся мелкие кристаллы имеют боченковидные или остропирамидальные формы. Обычно наблюдается в виде порошковатых и землистых примазок.
Цвет желтый, оранжево-желтый, темнооранжевый. Черта оранжево-желтая до кирпично-красной. Блеск алмазный.
Твердость 3-3,5. Хрупок. Спайность совершенная по {1120}. Уд. вес 4,9-5,0.
Диагностические признаки. От сходных с ним аурипигмента (As2S3), реальгара (AsS) и вульфенита (РbМоO4) отличается по поведению п. п. тр. (при сильном прокаливании с содой дает красно-бурый налет CdO). При растворении гринокита в кислотах чувствуется сильный запах H2S.Реакция на кадмий производится со спиртовым раствором дифенилкарбазида на фильтровальной бумаге.
Происхождение обычно экзогенное. Часто наблюдается в ассоциации с кадмийсодержащим сфалеритом или вюртцитом в зоне окисления сульфидных месторождении. Значительные скопления гринокита до сих пор не наблюдались.
Месторождения. Встречался в зоне окисления ряда месторождений: Кызыл-Эспе (Центральный Казахстан), Гайнах-Кан, Кан-Сай, Обисорбух (Средняя Азия). В виде мельчайших кристалликов в пустотах на халькопирите и галените был встречен в колчеданной залежи Сибаевского месторождения (Южн. Урал).
Из месторождений зарубежных стран должны быть отмечены: Пршибрам (Чехословакия), Фриденсвил в Пенсильвании (США) и др.
О применении кадмия см. сфалерит.
Киноварь - HgS. Предполагают, что название перешло из Индии, где так называются красная смола и "кровь дракона". Кубическая модификация HgS носит название метациннабарит.
Химический состав. Hg 86,2%, S 13,8%. Посторонние элементы обычно связаны с механическими примесями.
Сингония тригональная; тригонально-трапецоэдрический в. с. L33L2. Кристаллическая структура имеет гексагональный облик. В целом ее можно рассматривать как искаженную структуру NaCl с координационным числом 6 (как для Hg, так и для S). На деталях останавливаться не будем.
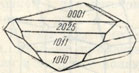
Рис. 97. Кристалл киновари
Облик кристаллов. Киноварь встречается в виде мелких толстотаблитчатых по {0001} или ромбоэдрических кристаллов {1011}, {2025} и др. (рис. 97), иногда с гранями трапецоэдра. Характерны двойники по {0001} (рис. 98). Агрегаты. Гораздо чаще наблюдается в виде вкрапленных неправильных по форме зерен, иногда в сплошных массах, а также в виде порошковатых примазок и налетов. Так называемая "печенковая руда" представляет собой скрытокристаллические массы, богатые посторонними землистыми и органическими примесями.
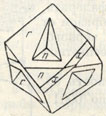
Рис. 98. Двойник киновари, r {1011}, n {2021}, x {4263}
Цвет киновари красный, иногда с свинцово-серой побежалостью. Черта красная. Блеск алмазный. Полупрозрачна.
Твердость 2-2,5. Хрупка. Спайность по {1010} довольно совершенная. Уд. вес 8,09-8,20. Прочие свойства. В отличие от метациннабарита, киноварь не проводит электричества.
Диагностические признаки. Киноварь довольно легко узнается по красному цвету, низкой твердости, высокому удельному весу и поведению п. п. тр.
П. п. тр. на угле возгоняется без остатка. Испарение начинается с температуры 200°. При нагревании в закрытой трубке образуется черный возгон, состоящий частью из HgS, частью из металлической ртути. При нагревании в открытой трубке, т. е. в присутствии кислорода, образуется металлическая ртуть, осаждающаяся на холодных стенках трубки в виде мельчайших шариков, по реакции: HgS +O2 = Hg+SO2. На этом основаны заводские методы получения ртути.
Растворяется в царской водке. Хлор вообще разлагает киноварь. Разлагается в растворах сульфидов едких щелочей; HNO3 и H2SO4 не действуют.
Происхождение. Месторождения киновари относятся исключительно к числу гидротермальных, образовавшихся при низких температурах. Известны примеры отложения киновари из горячих щелочных растворов, выходящих на поверхность земли (таковы, например, источники Стимбот в Неваде и Сольфор-Бэнк в Калифорнии, США). Из рудных минералов в ассоциации с киноварью встречаются: часто антимонит (Sb2S3), пирит, реже арсенопирит (FeAsS), реальгар (AsS), иногда сфалерит, халькопирит и др. Из нерудных минералов, сопровождающих выделения киновари, распространены обычно кварц, кальцит, нередко флюорит, барит, иногда гипс и др.
В зонах окисления ртутных месторождений как вторичные минералы встречаются: метациннабарит в виде черных пленок, самородная ртуть и изредка хлориды ртути. Вообще же киноварь в окислительной обстановке, в отличие от многих других сульфидов, довольно устойчива. Этим обстоятельством обусловливается тот факт, что она нередко присутствует в россыпях, при промывке которых благодаря высокому удельному весу легко улавливается в шлихах.
Практическое значение. Является почти единственным источником получения ртути. Самородная ртуть в природе встречается сравнительно редко. Ртуть употребляется преимущественно для амальгамации золота при добыче его из коренных руд, для изготовления химикалий, гремучей ртути Hg(CNO) - взрывчатого вещества для детонаторов, и в физических приборах.
Месторождения. Наиболее крупным месторождением в СССР является Никитовское (в 3 км от ст. Никитовка, Северо-Донецкой ж. д.). Здесь она встречается в ассоциации с антимонитом, кварцем, арсенопиритом и изредка пиритом.
Ряд небольших месторождений известен на Кавказе. Из них минералогический интерес представляет Хидешлепское, в котором киноварь ассоциирует с яркокрасным реальгаром (AsS).
Более значительные месторождения установлены в Средней Азии, главным образом вдоль северных предгоРbев Алайского и Туркестанского хребтов: Хайдарканское, Чаувайское и др. Киноварь находится здесь в ассоциации с кварцем, антимонитом, флюоритом, кальцитом, баритом и другими минералами в виде мелких зерен в рудных брекчиях.
Из иностранных месторождений большой известностью пользуются крупные месторождения Альмаден (Испания), Идрия(Италия).
|
ПОИСК:
|
© GEOMAN.RU, 2001-2021
При использовании материалов проекта обязательна установка активной ссылки:
http://geoman.ru/ 'Физическая география'
При использовании материалов проекта обязательна установка активной ссылки:
http://geoman.ru/ 'Физическая география'