
7. Группа рутила
В эту группу входят соединения типа АХ2, кристаллизующиеся в тетрагональной сингонии: двуокиси Ti, Sn, Мn и Pb. Из них ТiO2 в природе известна в трех полиморфных модификациях, носящих особые названия, а МnО2 - по крайней мере в двух модификациях. По некоторым данным, и соединение SNO2 является диморфным.
Все относящиеся сюда главные минералы не связаны друг с другом парагенетически и образуются в различных условиях. Двуокись олова отчасти встречается в условиях, аналогичных условиям, при которых образуется ТiO2, но в основном при геологических процессах ведет себя все же обособленно. МNO2 и РbO2 образуются в совершенно других условиях, почти исключительно при экзогенных процессах минералообразования.
Замечательной особенностью химического состава некоторых разностей рутила является то, что в них в виде изоморфных примесей присутствуют Nb5+ и Та5+ , но совместно с Fe2+ .
Химическая формула для таких разностей выражается в следующем виде: Ti3-3xNb2xFex•••O6. Из этой формулы видно, что два иона Nb5+ и один Fe2+ могут заменять три иона Ti4+ с сохранением общего заряда заменяемых ионов. Так как размеры ионных радиусов всех этих ионов примерно одного порядка (см. рис. 142), то кристаллическая структура минерала будет оставаться однотипной. Лишь размеры ее будут несколько возрастать соответственно размерам ионных радиусов Nb5+, Та5+ и Fe2+ (или Мn2). Таким образом, эти разности рутила представляют изоморфные смеси ТiO2, вернее Ti3O6, с Fe••Nb2O6 или Fe••Та2O6 (т. е. минералами, называемыми мосситом и тапиолитом), кристаллизующимися в той же структуре рутила.
Следует указать, что соединения FeNb2O6 и FeTa2O6 диморфны и кристаллизуются как в тетрагональной, так и в ромбической сингониях. Кристаллическая структура ромбической модификации (колумбита и танталита) также аналогична ромбической модификации ТiO2 (брукита).
Рутил - ТiO2. Название происходит от латинского слова "рутилус" - красноватый. Он является наиболее устойчивой модификацией ТiO2 как при высоких, так и при низких температурах.
Химический состав. Ti 60%. Химические анализы показывают, что в нем часто присутствуют примеси других элементов: Fe в виде закиси или окиси, иногда Sn4+ (до 1,5%), изредка Cr3+, V3+ и некоторые другие. Богатая FeTiO3 (в виде твердого раствора) разность называется нигрином.
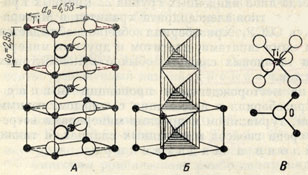
Рис. 158 Кристаллическая решетка рутила. А - в изображении центров ионов (черные кружки - титан, полые - кислород); по вертикали расположены три элементарные ячейки рутила. Б - в изображении октаэдров TiO6 (центральная колонка); ионы Ti располагаются внутри октаэдров. В - расположение ионов кислорода вокруг иона титана и титана вокруг кислорода
Сингония тетрагональная; дитетрагонально-дипирамидальный в. с. L44L25РС. Кристаллическая структура рутила, как типичная, изображена на рис. 158. Она отличается некоторыми особенностями. Если в кристаллической структуре типа корунда листы плотнейшей упаковки ионов кислорода располагаются перпендикулярно тройной оси, а в структуре типа шпинели - параллельно граням октаэдра (т. е. также перпендикулярно тройным осям), то в кристаллической структуре типа рутила, как показал Н. В. Белов, направления плотнейшей упаковки в виде колонок параллельны главной (четверной) оси кристаллов рутила. Каждый ион Ti окружается шестью ионами кислорода, располагающимися по углам почти правильного октаэдра (рис. 158-В), а каждый ион О окружен тремя ионами Ti (в углах почти равностороннего треугольника). Такие октаэдры в кристаллической структуре рутила вытянуты вдоль оси с в виде прямолинейных колонок (рис. 158-Б), чем и обусловливается игольчатый или шестоватый Облик кристаллов с направлениями плоскостей спайности параллельно вытянутости индивидов. Характерно, что в структуре рутила, в отличие от других модификаций TiO2, каждый октаэдр ТiO6 имеет по два ребра, общих с соседними октаэдрами (рис. 158-Б). Поскольку колонки плотно упакованных ионов кислорода, вытянутых вдоль четверной оси рутила, в сущности отвечают одному из трех возможных направлений в плоскости гексагональной плотнейшей упаковки, то не случайно, что для минералов группы рутила мы имеем коленчатой формы двойники и тройники срастания (рис.160) с углом, образуемым отдельными индивидами, близким к 120° (т. е. соответственно направлениям гексагональной сетки). Таким путем могут возникнуть даже кольцеобразные шестерники. Это же обстоятельство лежит в основе закономерных (под углом 120°) нарастаний тончайших иголочек или призматических кристалликов рутила на базальном пинакоиде {0001} гематита (см. рис. 148), слюды и других минералов, грани которых представлены плоскостями плотнейшей упаковки ионов кислорода. Облик кристаллов рутила чрезвычайно характерен: призматический, столбчатый до игольчатого. Обычные формы: {100}, {110}, {101), {111}, изредка {001}. Часто наблюдается штриховатость вдоль главной оси с. Типичные формы кристаллов изображены на рис. 159. Очень часты двойники коленчатой формы (рис. 160) с плоскостью срастания (011). Плоские сетчатые сростки двойников игольчатого рутила называют сагенитом. Как было указано, распространены закономерные срастания кристалликов рутила с кристаллами гематита, причем четверная ось рутила совпадает с одной из горизонтальных двойных осей гематита. Игольчатые волосовидные кристаллы рутила иногда наблюдаются в виде пучков, заключенных в прозрачных кристаллах кварца.
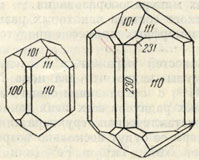
Рис. 159. Кристаллы рутила
Цвет рутила обычно темножелтый, бурый, красный и черный (нигрин). Бесцветные или бледноокрашенные разности исключительно редки. Черта желтая, светлобурая. Блеск алмазный до металловидного (для непрозрачных черных разностей). Ng=2,903 и Nm=2,616.
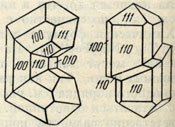
Рис. 160. Двойники рутила
Твердость 6. Хрупок. Спайность по {110} совершенная, по {100} средняя. Уд. вес 4,2-4,3.
Диагностические признаки. Весьма характерны тетрагональные призматического облика кристаллы и коленчатые двойники. Смешать можно с минералами, похожими по облику кристаллов: с цирконом (ZrSiO4), обладающим более высокой твердостью (7-8), и касситеритом (SNO2), для которого характерен высокий удельный вес. Волосовидные кристаллы рутила можно принять иногда за турмалин, отличающийся по оптическим константам.
П. п. тр. не плавится и не изменяется. В кислотах не растворяется. С фосфорной солью реагирует на титан (стекло в восстановительном пламени становится фиолетовым).
Происхождение. Рутил в природе образуется в различных условиях. Изредка он наблюдается как составная часть изверженных пород (сиенитов, реже гранитов). В небольших количествах он встречается в пегматитах и некоторых гидротермальных месторождениях в ассоциации с кварцем, минералами титана и железа (ильменитом, ильменорутилом, гематитом, магнетитом), иногда с корундом, силикатами и с другими минералами. Известны редкие находки его в виде новообразований в экзогенных продуктах разложения титановых минералов, изредка в осадочных породах, а также месторождениях боксита. Однако гораздо чаще он образуется при метаморфических процессах в результате преобразования титансодержащих минералов, выделяясь в виде самостоятельных зерен в гнейсах, слюдяных сланцах, амфиболитах и других породах. Весьма эффектны его игольчатые и волосовидные кристаллы в жилах альпийского типа, нередко заключенные в кристаллы горного хрусталя и гематита; часто он наблюдается в сопровождении брукита и анатаза.
В зоне окисления химически устойчив и нередко встречается в россыпях в виде окатанных зерен и галек.
Практическое значение. Употребляется для выплавки ферротитана, применяемого в производстве некоторых стойких при ударе сортов стали, в керамике в качестве бурой краски, в радиотехнике как детектор, для изготовления титановых белил и др.
Месторождения. В СССР рутил в виде крупных кристаллов известен в ряде месторождений в слюдяных сланцах, в пегматитовых жилах Ильменских гор, в месторождении Семиз-Бугу (Центральный Казахстан) с корундом и в других местах. Кроме того, он часто встречается в россыпях, особенно на Среднем Урале.
Из иностранных отметим месторождения С. Каролины (США), где встречаются замечательные кристаллы рутила различного облика.
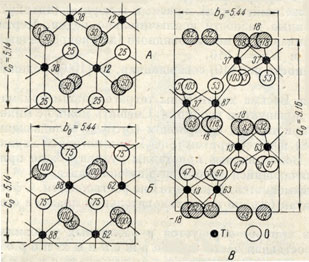
Рис. 161. Кристаллическая решетка брукита (в несколько идеализированном виде). А и Б - два участка решетки в проекции на (100); нижний располагается над верхним (ионы кислорода, помеченные цифрой 50, являются общими). В - решетка в проекции на (001) с действительным положением ионов кислорода и титана
Брукит-ТiO2. Сингония ромбическая, ромбо-дипирамидальный в. с. 3L23PC. Кристаллическая структура в несколько идеализированном виде представлена на рис. 161-А в проекции на плоскость (100), являющуюся плоскостью плотнейшей гексагональной упаковки ионов кислорода. На рис. 161-Б изображены вышележащие (над плоскостью чертежа) листы ионов кислорода (ср. цифры в кружках). Если наложить нижний рисунок на верхний, то не трудно убедиться в том, что в направлении оси а в целом мы имеем комбинацию гексагональной и кубической упаковок (топазовую упаковку): ионы кислорода "75" располагаются не над ионами "25", как следовало бы для плотнейшей гексагональной двуслойной упаковки, а так, как это имеет место в кубических плотнейших упаковках. Ионы Ti лежат между листами ионов кислорода в шестерном окружении, образуя зигзагообразные цепочки октаэдров в каждом слое плотнейшей упаковки. В отличие от структуры рутила, эти октаэдры здесь имеют по три общих ребра.
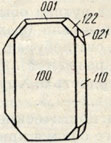
Рис. 162. Кристалл брукита
В соответствии со структурой находится и уплощенный но (100) облик кристаллов (рис. 162), причем четыре грани призмы {021}, параллельной оси а, и пинакоиды {001} образуют почти правильный шестиугольник в разрезе. Характерна также вертикальная штриховка на гранях.
Цвет брукита желто- или красно-бурый до черного. Черта бесцветная до серовато-или буровато-желтой. Блеск алмазный. Ng=2,741, Nm=2,586 и Np- 2,583. В некоторых образцах наблюдается очень сильное изменение показателей преломления, а в связи с этим меняется и дисперсия оптических осей для разных длин воли.
Твердость 5-6. Спайность по {110} несовершенная. Уд. вес 3,9-4,0 (меньше, чем рутила, но больше, чем анатаза). При прокаливании он увеличивается и становится равным удельному весу рутила (очевидно, происходит перестройка кристаллической решетки).
Месторождения. Превосходные кристаллы брукита у нас встречаются в Атлянской золотоносной россыпи близ Миасса и в жилах альпийского типа в ряде мест Урала.
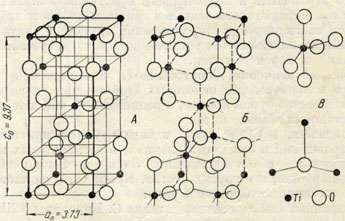
Рис. 163. Кристаллическая решетка анатаза. А - элементарная ячейка; Б - связи между Ti и О; В - расположение ионов кислорода вокруг иона титана и наоборот (ср. с рутилом - рис. 158)
Анатаз-TiO2. Сингония тетрагональная; дитетрагонально-дипирамидальный в. с. L44L25PC. Кристаллическая структура характеризуется плотнейшей кубической упаковкой ионов кислорода с вертикальной четверной осью (рис. 163). Координационные числа те же, что для рутила (6 : 3), но геометрические формы координации искаженные. Это обусловливается тем, что октаэдры ТiO6 сочетаются друг с другом таким образом, что имеют четыре общих ребра.
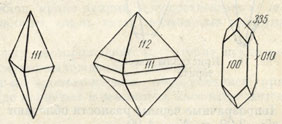
Рис. 164. Кристаллы анатаза
Кристаллы обладают характерным дипирамидальным обликом (рис. 164), причем дипирамида {111} острее дипирамиды (112}, близкой по форме к октаэдру. Реже встречаются кристаллы призматической и таблитчатой формы.
Цвет бурый, коричневый, черный. Черта бесцветная. Блеск алмазный. Nm =2,55 и Np =2,49.
Твердость 5-6. Спайность совершенная по {001} и {111}, чем отличается от рутила. Уд. вес 3,9 (меньше, чем рутила и брукита). П. п. тр. не плавится. В кислотах не растворяется.
Встречается в пегматитах и кристаллических сланцах (хлоритовых, слюдяных). Хорошо образованные кристаллы нередко наблюдаются на кварце в жилах альпийского тигa в Швейцарских Альпах, Бразилии, на С. Урале. Минерал химически устойчив, встречается в россыпях (Атлянская россыпь на Ю. Урале, около Миасса).
Касситерит - SNO2. "Касситерос" по-гречески - олово. Синоним: оловянный камень. Касситерит фактически является единственным промышленно важным минералом олова.
Химический состав. Sn 78,8% (по химической формуле). Почти постоянно присутствуют примеси. Во многих случаях, особенно в касситеритах из верматитовых месторождений, обнаруживаются Fe2O3, Та2O5, Nb2O5, ТiO2, МnО, FeO, изредка ZrO2 и WO3. Все эти разковалентные металлы, подобно тому как это встречается в некоторых разностях рутила, по всей вероятное и, присутствуют в виде изоморфных примесей.
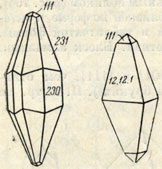
Рис. 165. Кристаллы касситерита
Сингония тетрагональная; дитетрагонально-дипирамидальный в. с. L44L25PC. Однако встречающиеся оптически двуосные разности, возможно, обладают кристаллической решеткой, близкой к ромбической. Искусственно ромбические кристаллы SNO2 (с уд. весом 6,70) были получены Добрэ. Кристаллическая структура идентична структуре рутила. Облик кристаллов. В виде хорошо образованных и сравнительно часто наблюдаемых кристаллов касситерит встречается в пустотах. Кристаллы обычно мелкие, по изредка достигают крупных размеров - до 10 см (в несколько килограммов весом). Чаще всего они имеют дипирамидалыный, пирамидально-призматический (рис. 165) или столбчатый облик, иногда игольчатый. В пегматитах обычно встречаются кристаллы дипирамидального облика и нередко в виде двойников. Вкрапленные зерна в грейзенах и гранитах часто обладают неправильными очертаниями. Неправильные формы свойственны также зернам касситерита, образовавшимся метасоматическим путем при эндогенном окислении станнина и других сернистых соединений олова. Двойники кристаллов очень часты и, подобно двойникам рутила, имеют коленчатый вид (рис. 166). Агрегаты. Сплошные зернистые массы встречаются редко. Обычно наблюдается в виде вкраплений кристалликов или неправильной формы зерен. В пустотах гидротермальных жил он иногда обнаруживается в виде друз хорошо образованных кристаллов. Так называемый "деревянистый касситерит" встречается в виде желваков и натечных форм; обладает концентрически-зональным строением, свойственным коллоидным массам.
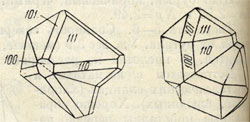
Рис. 166. Двойники касситерита
Цвет. Примесями Fe, Nb, Та и Мn касситерит обычно окрашен в темно-бурые оттенки до смоляно-черного цвета, причем в тонких шлифах часто наблюдается кристаллически-зональное строение отдельных кристаллов и зерен, обусловленное чередованием зон с различной степенью интенсивности окраски. Совершенно бесцветные разности очень редки. Черта у темных разностей обычно слабо окрашенная в буроватые оттенки. Блеск алмазный, в изломе - смоляной, слегка жирный. Грани кристаллов иногда матовые.
Непрозрачные черные разности обладают даже полуметаллическим блеском. Ng=2,09 и Nm =1,99.
Твердость 6-7. Хрупок. Спайность несовершенная, иногда ясная по {100}. Излом часто раковистый. Уд. вес 6,8-7,0. Прочие свойства. Не Maгнитен. Черные разности, обогащенные железом, все же обладают электромагнитными свойствами.
Диагностические признаки. По форме кристаллов, двойникам и цвету похож на рутил, а светлоокрашенные разности - также на циркон. Существенно отличается от них по удельному весу, твердости (у циркона 7-8) и характерному слегка жирному или смоляному блеску в изломе. В тонких шлифах мелкие зерна касситерита можно принять за циркон, двупреломление у которого значительно ниже.
П. п. тр. не плавится, но с тремя объемами соды на угле, при продолжительном дутье, в восстановительном пламени получаются мелкие ковкие корольки олова и белый налет SNO2. Кислоты не действуют. Если положить на касситерит каплю HCl и прикоснуться к нему кусочком цинка (или лучше специально изготовленной цинковой иглой), то через некоторое время под восстанавливающим влиянием бурно выделяющегося водорода на нем образуется металлический налет олова, блестящий после протирки на сукне (очень характерная, почти всегда удающаяся реакция для касситерита).
Происхождение. Месторождения касситерита генетически связаны с кислыми изверженными породами, преимущественно гранитами.
В самих гранитах касситерит устанавливается очень редко, и то главным образом в грейзенизированных участках, т. е. превращенных под влиянием пневматолитовых агентов (F,Cl, В и др.) в слюдисто-полево-шпато-кварцевую породу с топазом, флюоритом, лепидолитом (литиевой слюдой), турмалином и другими минералами. Полагают, что при высоких температурах олово переносится в виде летучих соединений SnF4 и SnCl4, которые впоследствии гидролизуются с выпадением SNO2. Установлено также, что щелочные растворы, содержащие сероводород, в восстановительной среде весьма активны в отношении переноса олова.
Очень неравномерно распространенные скопления касситерит образует в пегматитовых жилах, связанных с оловоносными интрузиями. В парагенезисе с ним присутствуют: кварц, слюды, альбит, турмалин, иногда колумбит, берилл, сподумен и т. д. Касситерит встречается также в некоторых контактово-метасоматических месторождениях в тесной ассоциации с различными сульфидами, что указывает на отложение его в гидротермальную стадию процесса.
Жильные гидротермальные месторождения касситерита являются гораздо более важными в промышленном отношении. Из них главное значение имеют типы жил: 1) кварцево-касситеритовые и 2) сульфиднокасситеритовые. В первом типе, кроме преобладающего кварца и касситерита, обычно присутствуют: турмалин, белая слюда, полевые шпаты, вольфрамит, в небольших количествах арсенопирит, пирит, иногда флюорит, топаз, берилл и другие минералы. Касситерит встречается главным образом вкрапленным в кварцевую массу и в пустотах в виде кристаллов, иногда достигающих крупных размеров. Во втором типе месторождений касситерит ассоциирует преимущественно с сульфидами: в одних случаях главным образом с пирротином и отчасти с сфалеритом, халькопиритом, станнином; в других - преимущественно с сфалеритом и галенитом и, наконец, в третьих - среди разнообразных сульфидов, где видную роль играет висмутин (боливийский тип). Из нерудных минералов, кроме кварца, в существенных количествах встречаются черные турмалины, очень часто железистые хлориты и карбонаты.
В зонах окисления оловорудных месторождений касситерит исключительно устойчив. Этим объясняется его нахождение в россыпях.
Касситерит экзогенного происхождения, образующийся при разрушении сульфидов олова, в виде пористых и землистых масс встречается в зонах окисления.
Практическое значение. Касситеритовые руды представляют собой единственный вид сырья, из которого в промышленных масштабах добывается олово. Последнее имеет следующие применения:
- для производства белой жести;
- для легкоплавких, трудноокисляемых сплавов с медью (бронзы), цинком, медью и свинцом (латуни), припоя (со свинцом) и др.;
- для лужения медной посуды;
- для изготовления оловянной фольги (станиоля);
- в керамика (для красок, эмали) и для других целей.
Месторождения. На территории СССР месторождения касситерита распространены главным образом в Восточной и особенно в Северо-Восточной Сибири. Укажем лишь на некоторые из них, наиболее типические.
- Представителем оловоносных пегматитов является 3авитинское месторождение (к юго-востоку от оз. Байкал, в районе слияния pp. Ингоды и Онона), где они залегают в краевых частях гранитного массива. Пегматитовые жилы здесь местами сильно изменены пневматолитовыми процессами, обусловившими оруденение. Измененные (грейзенизированные) участки их содержат розовый турмалин, лепидолит, гранат, касситерит и зеленый турмалин.
- К числу контактово-метасоматических месторождений относится Такфонское в Зеравшанском хребте (Средняя Азия), в котором среди скарновых образований с пирротином, арсенопиритом и халькопиритом встречаются касситерит, станнин и висмутин.
- Примером кварцево-касситеритовой формации является Ононское месторождение (ст. Онон, Забайкалье), где имеется ряд ветвящихся кварцевых жил, пересекающих осадочные породы. Руды представлены здесь кварцевыми массами, в которых касситерит ассоциирует с белой слюдой, топазом, флюоритом, арсенопиритом, пиритом и другими минералами.
- К касситерит-сульфидным месторождениям относятся Хапчерангинское (Восточное Забайкалье) и другие. Касситерит ассоциирует в них с различными сульфидами: арсенопиритом, пирротином, сфалеритом, вюртцитом, галенитом, халькопиритом, а также железистыми хлоритами, карбонатами и кварцем.
Из месторождений зарубежных стран большой известностью пользуется Малайская оловоносная провинция (Бирма, Западный Сиам, весь Малайский полуостров и южные острова - Баника, Билитон и другие), где широко распространены крупные касситеритсодержашие россыпи, образующиеся при разрушении коренных (главным сбразом пегматитовых и кварцево-касситеритовых) жил. В Боливии распространены кварцевые жилы с касситеритом, вольфрамовыми минералами, различными сульфидами, флюоритом и турмалином, а также сульфидно-касситеритовые месторождения.
Колумбит-танталит - (Fe,Mn)Nb2O6-(Fe,Mn)Ta2O6. Сбразуют непрерывный ряд изоморфных смесей. Название "колумбит" происходит от американского названия элемента ниобия - Колумбии. Синоним: ниобит.
Химический состав очень непостоянный. Даже в одном и том же месторождении содержания Fe и Мn, так же как и содержания Nb и Та, колеблются в широких пределах. Любопытно, что танталиты встречаются либо почти чисто марганцовистые, либо чисто железистые (промежуточные разности редки). Иногда в незначительных количествах содержат примеси: SnO2 (до 1-2%, реже до 2-9% в танталитах), W03, TiO2 и ZrO2, изредка UO2.
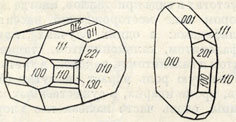
Рис. 167. Кристаллы колумбита
Сингония ромбическая: ромбо-дипирамидальный в. с. ЗL2ЗГС. Кристаллическая структура аналогична структуре брукита (см. рис. 161). Ионы Nb, Та, Мn, Fe, W, U и вероятно Sn располагаются на местах Ti, т. е. в центрах октаэдрических групп кислорода. Облик кристаллов пластинчатый по (010), таблитчатый, иногда короткостолбчатый (рис. 167). Наиболее обычные формы: пинакоиды {100}, {010}, {001}, призма {110}, дипирамида {111} и другие. Двойники наблюдаются по (201), нередко пластинчато-сердцевидные и характеризующиеся перистой штриховкой (рис. 168). Описаны закономерные срастания колумбита с самарскитом.
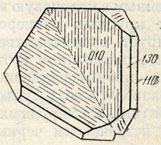
Рис. 168. Двойник колумбита
Цвет черный или буровато-черный. Черта красная или красновато-бурая до красновато-черной. Блеск полуметаллический. Непрозрачны.
Твердость 6. Хрупкие. Спайность по {100) довольно ясная. Уд. вес 5,15-8,20, увеличивается по мере увеличения содержания Та (рис. 169). Прочие свойства. Колумбит является проводником электричества.
Диагностические признаки. По внешним признакам распознать колумбит и танталит очень трудно. Их можно смешать:
- с ильменитом (отличие по цвету черты, облику кристаллов и отрицательным реакциям на Nb и Та);
- с вольфрамитом, обладающим более совершенной спайностью по {010} и меньшей твердостью;
- с ортитом, имеющим меньший удельный вес (3,2-4,2) и светлую черту;
- с самарскитом, эшинитом, эвксенитом и с другими ниобатами и танталатами, содержащими редкие земли и радиоактивные элементы, от которых без данных спектрального и радиометрического анализа, а также микрохимических реакций отличить их трудно.
П. п. тр. не плавятся. В кислотах не растворимы. Колумбит после сплавления с КОН и обработки разбавленной НСl и H2SO4, при прибавлении металлического Zn, дает устойчивую синюю окраску. Танталит после сплавления с KHSO4 и обработки НСl дает желтый раствор и тяжелый белый осадок, также приобретающий яркосиний цвет при прибавлении Zn; однако при разбавлении водой синяя окраска исчезает.
Происхождение. Обычно встречается в пегматитовых жилах в ассоциации с различными минералами, образующимися в более поздние стадии пегматитового процесса: альбитом, кварцем, мусковитом, турмалином, цирконом, вольфрамитом, касситеритом, иногда самарскитом, монацитом я другими.
Будучи относительно устойчивыми в зоне окисления минералами, они встречаются в россыпях.
Практическое значение. В случае значительных скоплений этих минералов, они могут иметь промышленное значение как источник ниобия и тантала, используемых в производстве особых сортов сталей и для других целей.
Месторождения. Из иностранных месторождений известны: месторождение около Мосса, Крагерё и Финбо (Норвегия), месторождения около Лиможа (Франция), а также месторождение Ивигтут (Гренландия), где встречены прекрасно образованные кристаллы, и др.
Пиролюзит - MNO2. "Пирос" по-гречески - огонь, "люзиос" - уничтожающий (употребляется в стеклоделии для уничтожения зеленого оттенка стекла). Синоним: полианит (так называли явнокристаллические разности).
Химический состав. Мn 63,2%, О 36,8%. В тонкозернистых и скрыто-кристаллических массах, обычно в виде механических примесей, присутствуют: Fe2O3, SiO2, Н2O и т. д.
Сингония тетрагональная; дитетрагонально-дипирамидальныи в. с. L44L25РС. Кристаллическая структура аналогична структуре рузила. В кристаллах встречается редко (только в пустотах). Они имеют игольчатый или шестоватый облик. Пиролюзит обычно наблюдается в сплошных кристаллических или скрытокристаллических, часто порошковатых, сажистых массах, частью в псевдоморфозах по почковидным агрегатам псиломелана.
Цвет пиролюзита черный. Иногда синеватая металлическая побежалость. Черта черная. Блеск полуметаллический. Непрозрачен.
Твердость у кристаллических индивидов 5-6; в агрегатах снижается до 2 (в зависимости от пористости и рыхлости их). Очень хрупок. Спайность совершенная по {110}, весьма характерна для пиролюзита. Уд. вес 4,7-5,0.
Диагностические признаки. От других черных марганцевых минералов, обладающих черной чертой, отличается по характерной для нею спайности, хрупкости и сравнительно низкой твердости.
П. п. тр. не плавится. Выделяя часть кислорода (до 12% весовых), переходит в низшие окислы и буреет. При нагревании до 500° не изменяется; в интервале 550-650°, как установлено рентгенометрическими исследованиями, происходит диссоциация с образованием β-браунита (кубической модификации); при дальнейшем нагревании при температурах 940-1100° β-браунит переходит в наиболее устойчивый при высоких температурах гаусманит.
В НСl растворяется с выделением хлора. Это явление широко используется в химической промышленности. С бурой и фосфорной солью в окислительном пламени дает фиолетовое стекло; при восстановлении оно становится бесцветным.
Происхождение. Сравнительно редко образуется в гидротермальных месторождениях марганца, и лишь при условии явно окислительной среды. Зато широко распространен на земной поверхности как высший природный окисел марганца в прибрежных фациях осадочных месторождений. Является наиболее устойчивым окислом марганца в зоне окисления. В этих условиях в него в конце концов переходят все марганцевые минералы, содержащие марганец в низших степенях окисления. Поэтому нередки псевдоморфозы пиролюзита по манганиту, вернадиту, псиломелану, гаусманиту и др. Вследствие своей хрупкости, в россыпях встречается крайне редко.
Практическое значение. Чисто пиролюзитовые руды используются для самых различных целей:
- в производстве сухих электрических батарей;
- в изготовлении для той же цели искусственно активированных продуктов;
- в стекольном деле для обесцвечивания зеленого стекла;
- при изготовлении химических препаратов, употребляемых в медицине и для других целей;
- в производстве специальных противогазов для защиты от окиси углерода, катализаторов типа гопкалита для очистки от вредных примесей в выхлопных газах автомобильных двигателей и пр.;
- в технике при производстве олифы, масел, воска, в кожевенном деле при выделке хромовой кожи, в фотографии, в производстве красок и т. д. Для целей производства сухих батарей содержание двуокиси марганца в руде должно быть не ниже 80%.
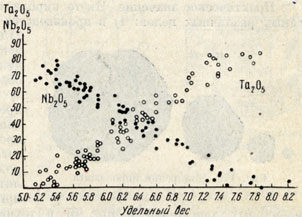
Рис. 169. Зависимость между содержанием Та2О5 и Nb2О5 и удельным весом. По А. И. Гинзбургу
Месторождения. Постоянно встречается во всех так называемых марганцевых шляпах, т. е. в зонах окисления, а также в ряде осадочных месторождений. Из числа крупнейших в мире осадочных месторождений на нашей территории необходимо отметить Чиатурское (Грузинская ССР), в котором пиролюзит слагает ослитовые стяжения и, кроме того, в виде скрытокристаллических мягких агрегатов образует псевдоморфозы по оолитам манганита (на выходах пластов на поверхность), Никопольское (Украина), где он иногда слагает более крупные шаровидные конкреции (рис. 170) с концентрически-зональным строением.

Рис. 170. Конкреции пиролюзита
Из иностранных месторождений следует отметить зоны окисления метаморфизованных месторождений Индии, Золотого Берега (Западная Африка) и др. Хорошо образованные кристаллы были установлены в месторождении Платтен в Богемии (Чехословакия).
|
ПОИСК:
|
© GEOMAN.RU, 2001-2021
При использовании материалов проекта обязательна установка активной ссылки:
http://geoman.ru/ 'Физическая география'
При использовании материалов проекта обязательна установка активной ссылки:
http://geoman.ru/ 'Физическая география'